Seroprevalencia de Trypanosoma cruzi en niños de Veracruz, México: línea epidemiológica de base para un modelo de control fundamentado de la transmisión activa de la enfermedad de Chagas
Resumen
Introducción. En el 2021, la Secretaría de Salud de México y la Organización Panamericana de la Salud lanzaron una iniciativa para interrumpir la transmisión vectorial intradomiciliaria de Trypanosoma cruzi, fundamentada en la prevalencia de la enfermedad de Chagas en la población infantil. El estado mexicano de Veracruz fue el pionero de esta iniciativa.
Objetivo. Estimar la seroprevalencia de infección por T. cruzi en menores de 15 años de localidades rurales de Veracruz, México.
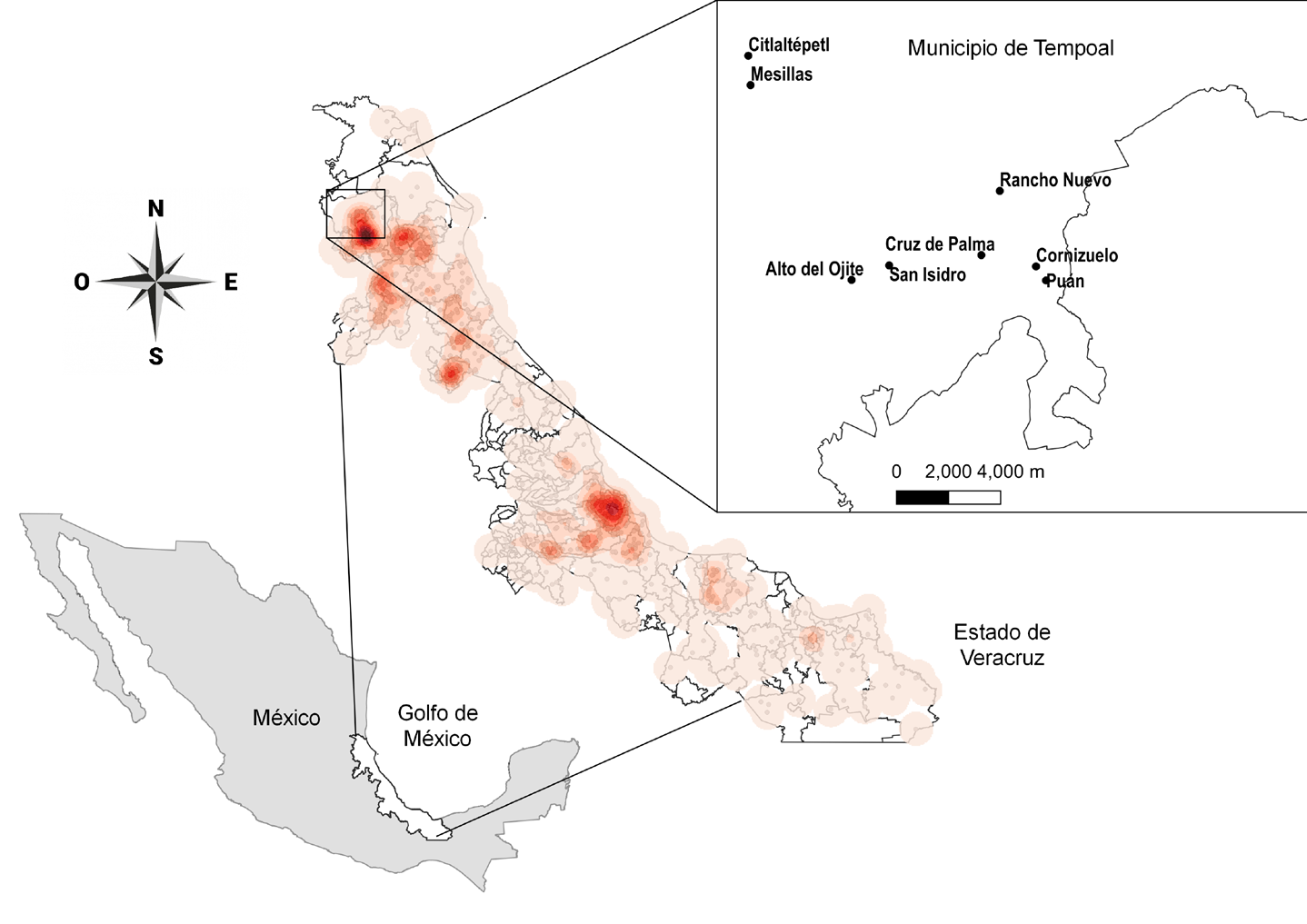
Materiales y métodos. Se identificaron ocho localidades prioritarias para la serología basal del municipio de Tempoal, Veracruz. Entre junio y agosto de 2017, se recolectaron muestras de sangre en papel filtro de 817 individuos para su tamizaje mediante un inmunoensayo enzimático de tercera generación. Los casos reactivos del tamizaje se confirmaron mediante pruebas de hemaglutinación indirecta, ensayo de inmunoabsorción ligado a enzimas e inmunofluorescencia indirecta en muestras de suero. Se calculó la seroprevalencia y su intervalo de confianza (IC) del 95 %.
Resultados. En las localidades de Citlaltépetl, Cornizuelo, Cruz de Palma y Rancho Nuevo se confirmaron casos de la enfermedad de Chagas en menores de 15 años con una seroprevalencia de 1,9 % (IC 95 % = 1,12-3,16).
Conclusiones. Los resultados indican que estas comunidades presentan transmisión reciente de T. cruzi y permiten establecer una línea epidemiológica de base para el diseño e implementación de un modelo dirigido a aquellas áreas geográficas con transmisión activa. Se espera que dicho modelo contribuya a la eliminación de la transmisión vectorial intradomiciliaria del tripanosomátido en México.
Descargas
Referencias bibliográficas
Pérez-Molina JA, Molina I. Chagas disease. Lancet. 2018;391:82-94. https://doi.org/10.1016/S0140-6736(17)31612-4
Organización Panamericana de la Salud. Control, interrupción de la transmisión y eliminación de la enfermedad de Chagas como problema de salud pública. Guía de evaluación, verificación y validación. Washington, D.C.: OPS; 2019. p. 76.
Instituto de Diagnóstico y Referencia Epidemiológicos. Lineamientos de vigilancia por laboratorio de la enfermedad de Chagas. Ciudad de México. Fecha de consulta: 24 de agosto del 2022. Disponible en: https://www.gob.mx/cms/uploads/attachment/file/483705/Lineamientos_Chagas__4T.pdf
Secretaría de Salud. Manual de procedimientos para la enfermedad de Chagas en México. Fecha de consulta: 24 de agosto del 2022. Disponible en: https://www.gob.mx/cms/uploads/attachment/file/447946/Manual_de_Procedimientos_para_la_Enfermedad_de_Chagas_en_Mexico.pdf
Diario Oficial de la Federación. NOM-253-SSA1-2012 - Para la disposición de sangre humana y sus componentes con fines terapéuticos. Fecha de consulta: 26 de agosto del 2022. Disponible en: http://www.cnts.salud.gob.mx/descargas/NOM-253-SSA1-2012.pdf
Dirección General de Epidemiología. Manual de procedimientos estandarizados para la vigilancia epidemiológica de las enfermedades transmitidas por vectores. Fecha de consulta: 24 de agosto del 2022. Disponible en: https://epidemiologia.salud.gob.mx/gobmx/salud/documentos/manuales/36_Manual_ETV.pdf
Sistema Único de Información. Sistema Nacional de Vigilancia Epidemiológica. Boletín Epidemiológico 2017-2021. Fecha de consulta: 31 de agosto del 2022. Disponible en: https://www.gob.mx/salud/acciones-y-programas/historico-boletin-epidemiologico
Organización Panamericana de la Salud. X Reunión de la Comisión Intergubernamental de la Iniciativa Andina de Control de la Transmisión Vectorial y Transfusional y la Atención Médica de la Enfermedad de Chagas. Fecha de consulta: 26 de agosto del 2022. Disponible en: https://www.paho.org/en/file/38308/download?token=gFAqvX45
Salazar-Schettino PM, Cravioto QA, Tapia-Conver R. Mexico iniciative: A proposal for the epidemiological control and surveillance of Chagas disease in Mexico. Bol Chil Parasitol. 2001;56:76-9. https://doi.org/10.4067/S0365-94022001000200008
Gamboa-León R, Ramírez-González C, Pacheco-Tucuch FS, O’Shea M, Rosecrans K, Pippitt J, et al. Seroprevalence of Trypanosoma cruzi among mothers and children in rural Mayan communities and associated reproductive outcomes. Am J Trop Med Hyg. 2014;91:348-53. https://doi.org/10.4269/ajtmh.13-0527
Salazar PM, Rojas G, Bucio M, Cabrera M, García G, Ruiz A, et al. Seroprevalencia de anticuerpos contra Trypanosoma cruzi y su asociación con factores de riesgo en menores de 18 años de Veracruz, México. Rev Panam Salud Pública. 2007;22:75-82.
Salvatella R, Rosa R, González M, Basmadjián Y, Combol A, Benavidez U, et al. Seroprevalence of T. cruzi infection in six and twelve year-old school children from three Uruguayan endemic departments. Bol Chil Parasitol. 1999;54:51-6. https://doi.org/10.4067/S0365-94021999000300003
Sales-Junior PA, Molina I, Fonseca-Murta SM, Sánchez-Montalvá A, Salvador F, Corrêa-Oliveira R, et al. Experimental and clinical treatment of Chagas disease: A review. Am J Trop Med Hyg. 2017;97:1289-303. https://doi.org/10.4269/ajtmh.16-0761
Centro Nacional de Programas Preventivos y Control de Enfermedades. Programa de acción específico del programa de prevención y control de enfermedades transmitidas por vectores e intoxicación por veneno de artrópodos 2020-2024. Fecha de consulta: 24 de agosto del 2022. Disponible en: https://www.gob.mx/salud/documentos/programa-deaccion-especificao
Secretaría de Salud. Estrategia de intervención nacional para la interrupción de la transmisión vectorial intradomiciliaria de la enfermedad de Chagas en México. Ciudad de México: SESVER, CENAPRECE, OPS, UADY; 2021. p. 76. https://www.gob.mx/cms/uploads/attachment/file/819576/Estrategia_de_intervencio_n_nacional_para_la_Interrupcio_n_de_la_transmisio_n_vectorial_intradomiciliaria_de_la_enfermedad_de_Chagas_en_Me_xico.pdf
Salazar-Schettino PM, Rojas-Wastavino GE, Cabrera-Bravo M, Bucio-Torres MI, Martínez-Ibarra JA, Monroy-Escobar MC, et al. A revision of thirteen species of Triatominae (Hemiptera: Reduvidae) vectors of Chagas disease in Mexico. J Selva Andina Res Soc. 2010;1:57-80.
Servicios de Salud de Veracruz. Base de datos del Programa de Prevención y Control de la Enfermedad de Chagas. Xalapa: Servicios de Salud de Veracruz; 2022.
Diario Oficial de la Federación. NOM-032-SSA2-2014 - Para la vigilancia epidemiológica, promoción, prevención y control de las enfermedades transmitidas por vectores. Fecha de consulta: 26 de agosto del 2022. Disponible en: https://www.dof.gob.mx/nota_detalle.php?codigo=5389045&fecha=16/04/2015#gsc.tab=0
Sistema de Información Municipal. Cuadernillos Municipales, 2016. Fecha de consulta: 25 de agosto del 2022. Disponible en: http://ceieg.veracruz.gob.mx/wp-content/uploads/sites/21/2016/05/Tempoal.pdf
Velasco-Castrejón O, Valdespino JL, Tapia-Conyer R, Salvatierra B, GuzmánBracho C, Magos C, et al. Seroepidemiología de la enfermedad de Chagas en México. Salud Pública Mex. 1992;34:186-96.
Guzmán-Bracho C, García-García L, Floriani-Verdugo J, Guerrero-Martínez S, Torres-Cosme M, Ramírez-Melgar C, et al. Riesgo de transmisión de Tripanosoma cruzi por transfusión de sangre en México. Rev Panam Salud Pública. 1998;4:94-9.
Arnal A, Waleckx E, Rico-Chávez O, Herrera C, Dumonteil E. Estimating the current burden of Chagas disease in Mexico: A systematic review and meta-analysis of epidemiological surveys from 2006 to 2017. PloS Negl Trop Dis. 2019;13:e0006859. https://doi.org/10.1371/journal.pntd.0006859
Estrada-Franco JG, Bhatia V, Díaz-Albiter H, Ochoa-García L, Barbabosa A, Vázquez-Chagoyan JC, et al. Human Trypanosoma cruzi infection and seropositivity in dogs, México. Emerg Infect Dis. 2006;12:624-30. https://doi.org/10.3201/eid1204.050450
Juárez-Tobías S, Vaughan G, Torres-Montoya A, Escobar-Gutiérrez A. Seroprevalence of Trypanosoma cruzi among Teenek Amerindian residents of the Huasteca region in San Luis Potosí, México. Am J Trop Med Hyg. 2009;81:219-22.
Mazariego-Arana MA, Monteón VM, Ballinas-Verdugo MA, Hernández-Becerril N, Alejandre-Aguilar R, Reyes PA. Seroprevalence of human Trypanosoma cruzi infection in different geographic zones of Chiapas, México. Rev Soc Bras Med Trop. 2001;34:453-8. https://doi.org/10.1590/S0037-86822001000500008
Newton-Sánchez OA, Espinoza-Gómez F, Melnikov V, Delgado-Enciso I, Rojas-Larios F, Dumonteil E, et al. Seroprevalence of Trypanosoma cruzi (TC) and risk factors in Colima, México. Gac Med Mex. 2017;153:179-84.
Olivera-Mar A, Guillén-Ortega F, Cruz-Vidal S, Hernández-Becerril N, PérezGaldamez E, Córdova-Concepción G, et al. Serological and parasitological screening of Trypanosoma cruzi infection in mothers and newborns living in two Chagasic areas of México. Arch Med Res. 2006;37:774-7. https://doi.org/10.1016/j.arcmed.2006.02.006
Segura EL, Escobar-Mesa A. Epidemiología de la enfermedad de Chagas en el estado de Veracruz. Salud Pública Mex. 2005;47:201-8.
Banco Interamericano de Desarrollo, Organización Panamericana de la Salud, International Development Research Center, Comisión Nacional Honoraria de Zoonosis del Ministerio de Salud Pública de Uruguay. Programa Regional para el Control de la Enfermedad de Chagas en América Latina. Lineamientos y recomendaciones técnicas y de política pública para el abordaje de la enfermedad de Chagas. Montevideo, Uruguay: BID; 2010. p. 84.
Algunos artículos similares:
- Patricia Escobar, Katherine Paola Luna, Indira Paola Hernández, César Mauricio Rueda, María Magdalena Zorro, Simon L. Croft, Susceptibilidad in vitro a hexadecilfosfocolina (miltefosina), nifurtimox y benznidazole de cepas de Trypanosoma cruzi aisladas en Santander, Colombia , Biomédica: Vol. 29 Núm. 3 (2009)
- María Clara Echeverry, Nubia Catalina Tovar, Guillermo Mora, Presencia de anticuerpos contra neurorreceptores cardiacos de acetilcolina muscarínicos tipo II en pacientes con enfermedad de Chagas e implantación de marcapasos , Biomédica: Vol. 29 Núm. 3 (2009)
- Marlene Reyes, Víctor Manuel Angulo, Ciclo de vida de Triatoma dimidiata Latreille, 1811 (Hemiptera, Reduviidae) en condiciones de laboratorio: producción de ninfas para ensayos biológicos , Biomédica: Vol. 29 Núm. 1 (2009)
- Azael Saldaña, José E. Calzada, Juan Garisto, Salomón Zebedes, Franklyn E. Samudio, Roberto Blandón, Óscar Avilés, Prevalencia de autoanticuerpos contra receptores autonómicos en pacientes panameños con cardiopatía chagásica crónica y con otras formas de cardiopatía , Biomédica: Vol. 29 Núm. 1 (2009)
- Concepción Judith Puerta, Johana María Guevara, Paula Ximena Pavía, Marleny Montilla, Rubén Santiago Nicholls, Edgar Parra, Yuli Katherine Barrera, Evaluación de las pruebas de PCR TcH2AF-R y S35-S36 para la detección de Trypanosoma cruzi en tejido cardiaco de ratón , Biomédica: Vol. 28 Núm. 4 (2008)
- Jairo Echeverry, Carlos Mauricio Hurtado, Myriam Gutiérrez, Aspectos clínicos y niveles de plomo en niños expuestos de manera paraocupacional en el proceso de reciclaje de baterías de automóviles en las localidades de Soacha y Bogotá, D.C. , Biomédica: Vol. 28 Núm. 1 (2008)
- Concepción Judith Puerta, Paula Ximena Pavia, Marleny Montilla, Carolina Flórez, Giomar Herrera, Juan Manuel Ospina, Fred Manrique, Rubén Santiago Nicholls, Reporte del primer caso de enfermedad de Chagas transplacentaria analizado por AP-PCR en Moniquirá, Boyacá , Biomédica: Vol. 29 Núm. 4 (2009)
- Keila Torres, Francys Avendaño-Rangel, Eliécer Lizano, María Rojas, Claudina Rodríguez-Bonfante, Rafael Bonfante-Cabarcas, Elis Aldana, Evaluación de la estructura espacial de Triatoma maculata del centro-occidente de Venezuela y su viabilidad alimentado con sangre humana en condiciones de laboratorio , Biomédica: Vol. 30 Núm. 1 (2010)
- José Alejandro Martínez-Ibarra, Jorge Alejandro Martínez-Grant, Miguel Roberto Verdugo-Cervantes, Rafael Bustos-Saldaña, Benjamín Nogueda-Torres, Vigilancia de la presencia de triatominos mediante gallineros en el sur de Jalisco, México , Biomédica: Vol. 30 Núm. 1 (2010)
- Nelson Grisales, Omar Triana, Víctor Angulo, Nicolás Jaramillo, Gabriel Parra-Henao, Francisco Panzera, Andrés Gómez-Palacio, Diferenciación genética de tres poblaciones colombianas de Triatoma dimidiata (Latreille, 1811) mediante análisis molecular del gen mitocondrial ND4 , Biomédica: Vol. 30 Núm. 2 (2010)
Derechos de autor 2024 Biomédica

Esta obra está bajo una licencia internacional Creative Commons Atribución 4.0.
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























