Mutaciones del gen ARN ribosómico 23S de Helicobacter pylori asociadas con resistencia a claritromicina en pacientes atendidos en una unidad de endoscopia de Medellín, Colombia
Resumen
Introducción. La claritromicina es el antibiótico de primera línea para el tratamiento de la infección por Helicobacter pylori. La resistencia bacteriana se produce principalmente por mutaciones puntuales del gen ARN ribosómico 23S (ARNr 23S).
Objetivo. Determinar la frecuencia de las mutaciones puntuales A2143G y A2142G del gen ARNr 23S asociadas con la resistencia de H. pylori a la claritromicina en muestras de pacientes con manifestaciones dispépticas en Medellín, región noroccidental de Colombia.
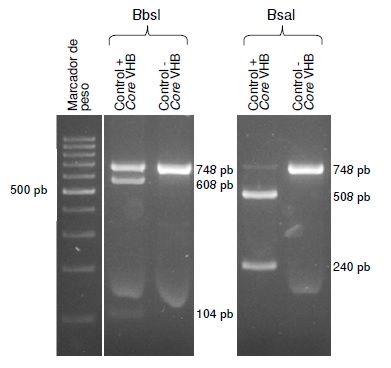
Materiales y métodos. Se extrajo ADN a partir de muestras de biopsia gástrica obtenidas de pacientes con manifestaciones dispépticas atendidos en una unidad de endoscopia entre el 2016 y el 2017. Mediante reacción en cadena de la polimerasa (PCR), se amplificaron las regiones s y m del gen vacA y una región del gen ARNr 23S bacteriano. La presencia de las mutaciones A2142G y A2143G se determinó por la técnica de polimorfismos de longitud de fragmentos de restricción (RFLP) con las enzimas BbsI y BsaI, respectivamente.
Resultados. Se encontró una prevalencia de infección de 44,2 % (175/396), según el informe de histopatología. En 143 de estas 175 muestras positivas se amplificaron las tres regiones del genoma bacteriano. Se identificaron las mutaciones A2143G y A2142G en 27 muestras (18,8 %; 27/143), la mutación más frecuente fue la A2143G (81,5 %; 22/27).
Conclusiones. Hubo una gran prevalencia de mutaciones asociadas con la resistencia de H. pylori a la claritromicina en la población de estudio. Se requieren estudios adicionales para establecer la resistencia bacteriana en la población colombiana y, así, determinar los tratamientos de primera línea y de rescate.
Descargas
Referencias bibliográficas
IARC Working Group on the Evaluation of Carcinogenic Risks to Humans. IARC monographs on the evaluation of carcinogenic risks to humans. Volume 100. A review of human carcinogens. Part B. Biological agents. Lyon: International Agency for Research on Cancer; 2012. p. 385-435.
Kao CY, Sheu BS, Wu JJ. Helicobacter pylori infection: An overview of bacterial virulence factors and pathogenesis. Biomed J. 2016;39:14-23. https://doi.org/10.1016/j.bj.2015.06.002
Zabala B, Lucero Y, Lagomarcino AJ, Orellana-Manzano A, George S, Torres JP, et al. Prevalence and dynamics of Helicobacter pylori infection during childhood. Helicobacter. 2017;22:e12399. https://doi.org/10.1111/hel.12399
Hunt RH, Xiao SD, Megraud F, León-Barua R, Bazzoli F, van Der Merwe S, et al. Helicobacter pylori in developing countries. World Gastroenterology Organisation Global Guideline. J Gastrointestin Liver Dis. 2011;20:299-304.
Hooi JK, Lai WY, Ng WK, Suen MM, Underwood FE, Tanyingoh D, et al. Global prevalence of Helicobacter pylori Infection: Systematic review and meta-analysis. Gastroenterology. 2017;153:420-9. https://doi.org/10.1053/j.gastro.2017.04.022
Wroblewski LE, Peek RM, Wilson KT, Wilson KT. Helicobacter pylori and gastric cancer: Factors that modulate disease risk. Clin Microbiol Rev. 2010;23:713-39. https://doi.org/10.1128/CMR.00011-10
Gisbert JP. Enfermedades relacionadas con la infección por Helicobacter pylori. Gastroenterol Hepatol. 2013;36:39-50.
Ferlay J, Soerjomataram I, Ervik M, Dikshit R, Eser S, Mathers C, et al. GLOBOCAN 2012 v1.0, Cancer incidence and mortality worldwide: IARC Cancerbase No. 11. Lyon: International Agency for Research on Cancer; 2013.
Malfertheiner P, Megraud F, O’Morain CA, Gisbert JP, Kuipers EJ, Axon AT, et al. Management of Helicobacter pylori infection-the Maastricht V/Florence Consensus Report. Gut. 2017;66:6-30. https://doi.org/10.1136/gutjnl-2016-312288
Martínez JD, Henao SC, Lizarazo JI. Antibiotic resistance of Helicobacter pylori in Latin America and the Caribbean. Rev Colomb Gastroenterol. 2014;29:218-27.
Versalovic J, Osato MS, Spakovsky K, Dore MP, Reddy R, Stone GG, et al. Point mutations in the 23S rRNA gene of Helicobacter pylori associated with different levels of clarithromycin resistance. J Antimicrob Chemother. 1997;40:283-6.
Trespalacios AA, Rimbara E, Otero W, Reddy R, Graham DY. Improved allele-specific PCR assays for detection of clarithromycin and fluoroquinolone resistant of Helicobacter pylori in gastric biopsies: Identification of N87I mutation in GyrA. Diagn Microbiol Infect Dis. 2015;81:251-5. https://doi.org/10.1016/j.diagmicrobio.2014.12.003
Ciftci IH, Ugras M, Acartekin G, Asik G, Safak B, Dilek FH. Comparison of FISH, RFLP and agar dilution methods for testing clarithromycin resistance of Helicobacter pylori. Turkish J Gastroenterol. 2015;25:75-80. https://doi.org/10.5152/tjg.2014.4688
Trespalacios AA, Otero W, Caminos JE, Mercado MM, Ávila J, Rosero LE, et al. Phenotypic and genotypic analysis of clarithromycin-resistant Helicobacter pylori from Bogotá, D.C., Colombia. J Microbiol. 2013;51:448-52. https://doi.org/10.1007/s12275-013-2465-6
Kim KS, Kang JO, Eun CS, Han DS, Choi TY. Mutations in the 23S rRNA gene of Helicobacter pylori associated with clarithromycin resistance. J Korean Med Sci. 2002;17:599-603. https://doi.org/10.3346/jkms.2002.17.5.599
Trespalacios AA, Otero-Regino W, Mercado-Reyes M. Helicobacter pylori resistance to metronidazole, clarithromycin and amoxicillin in Colombian patients. Rev Colomb Gastroenterol. 2010;25:29-36.
Bravo LE, Cortés A, Carrascal E, Jaramillo R, García LS, Bravo PE, et al. Helicobacter pylori: patología y prevalencia en biopsias gástricas en Colombia. Colomb Med. 2003;34:124-31.
Lee YC, Liou JM, Wu MS, Wu CY, Lin JT. Eradication of Helicobacter pylori to prevent gastroduodenal diseases: Hitting more than one bird with the same stone. Therap Adv Gastroenterol. 2008;1:111-20. https://doi.org/10.1177/1756283X08094880
Instituto Nacional de Salud. Quinto Informe ONS: carga de enfermedad por enfermedades crónicas no transmisibles y discapacidad en Colombia. Quinta edición. Bogotá: Instituto Nacional de Salud; 2015.
Regino WO. La importancia de cultivar Helicobacter pylori. Rev Colomb Gastroenterol. 2013;28:87-92.
Sierra F, Forero JD, Rey M. Tratamiento ideal del Helicobacter pylori: una revisión sistemática. Rev Gastroenterol Mex. 2014;79:28-49. https://doi.org/10.1016/j.rgmx.2013.03.003
Gómez M, Ruíz O, Páramo-Hernández D, Albis R, Sabbagh LC. Erradicación del Helicobacter pylori: encuesta realizada por la Asociación Colombiana de Gastroenterología. Rev Col Gastroenterol. 2015;30:25-31.
Camargo MC, García A, Riquelme A, Otero W, Camargo CA, Hernández-García T, et al. The problem of Helicobacter pylori resistance to antibiotics: A systematic review in Latin America. Am J Gastroenterol. 2014;109:485-95. https://doi.org/10.1038/ajg.2014.24
Di Ciaula A, Scaccianoce G, Venerito M, Zullo A, Bonfrate L, Rokkas T, et al. Eradication rates in italian subjects heterogeneously managed for Helicobacter pylori infection. Time to abandon empiric treatments in Southern Europe. J Gastrointest Liver Dis. 2017;26:129-37. https://doi.org/10.15403/jgld.2014.1121.262.itl
Castaño R, Ruiz-Vélez MH, Martínez-Hincapié C, Naranjo-Aristizábal FA, Campuzano-Maya G, Sanín-Fonnegra E, et al. Evaluación para comparar dos esquemas de terapia estándar (7 frente a 10 días) contra el Helicobacter pylori, con seguimiento clínico a 1 año. Rev Colomb Gastroenterol. 2012;27:80-7.
Castaño R, Ruiz-Vélez MH, Campuzano-Maya G, Sanín-Fonnegra E, Puerta-Díaz JD, Calvo-Betancur V, et al. Randomized study comparing standard first line 10 day therapy against Helicobacter pylori including clarithromycin versus standard first line therapy with levofloxacin. Rev Colomb Gastroenterol. 2013;28:101-8.
Correa S, Cardona AF, Correa T, Correa LA, García HI, Estrada S. Prevalence of Helicobacter pylori and histopathological features in gastric biopsies from patients with dyspeptic symptoms at a referral center in Medellín. Rev Colomb Gastroenterol. 2016;31:9-15.
Peixoto A, Silva M, Pereira P, Macedo G. Biopsies in gastrointestinal endoscopy: When and how. GE Port J Gastroenterol. 2016;23:19-27. https://doi.org/10.1016/j.jpge.2015.07.004
Genta RM, Graham DY. Comparison of biopsy sites for the histopathologic diagnosis of Helicobacter pylori: A topographic study of H. pylori density and distribution. Gastrointest Endosc. 1994;40:342-5. https://doi.org/10.1016/S0016-5107(94)70067-2
Acosta CP, Hurtado FA, Trespalacios AA. Determinación de mutaciones de un solo nucleótido en el gen 23S rRNA de Helicobacter pylori relacionadas con resistencia a claritromicina en una población del departamento del Cauca, Colombia. Biomédica. 2013;34:156-62. https://doi.org/10.7705/biomedica.v34i0.1649
Occhialini A, Urdaci M, Doucet-Populaire F, Bébéar CM, Lamouliatte H, Mégraud F. Macrolide resistance in Helicobacter pylori: Rapid detection of point mutations and assays of macrolide binding to ribosomes. Antimicrob Agents Chemother. 1997;41:2724-8. https://doi.org/10.1128/AAC.41.12.2724
Rendón JC, Cortés-Mancera F, Restrepo-Gutiérrez JC, Hoyos S, Navas MC. Molecular characterization of occult hepatitis B virus infection in patients with end-stage liver disease in Colombia. PLoS One. 2017;12:e0180447. https://doi.org/10.1371/journal.pone.0180447
Patel SK, Pratap CB, Jain AK, Gulati AK, Nath G. Diagnosis of Helicobacter pylori: What should be the gold standard? World J Gastroenterol. 2014;20:12847-59. https://doi.org/10.3748/wjg.v20.i36.12847
Jiménez F, Barbaglia Y, Bucci P, Tedeschi FA, Zalazar FE. Detección molecular y genotipificación de Helicobacter pylori en biopsias gástricas de pacientes adultos sintomáticos de la ciudad de Santa Fe, Argentina. Rev Argent Microbiol. 2013;45:39-43.
Wang YK, Kuo FC, Liu CJ, Wu MC, Shih HY, Wang SS, et al. Diagnosis of Helicobacter pylori infection: Current options and developments. World J Gastroenterol. 2015;21:11221-35. https://doi.org/10.3748/wjg.v21.i40.11221
de Martel C, Plummer M, van Doorn LJ, Vivas J, López G, Carillo E, et al. Comparison of polymerase chain reaction and histopathology for the detection of Helicobacter pylori in gastric biopsies. Int J Cancer. 2010;126:1992-6. https://doi.org/10.1002/ijc.24898
Cosgun Y, Yildirim A, Yucel M, Karakoc AE, Koca G, Gonultas A, et al. Evaluation of invasive and noninvasive methods for the diagnosis of Helicobacter pylori infection. Asian Pac J Cancer Prev. 2016;17:6165-72. https://doi.org/10.22034/APJCP.2016.17.12.5265
Hammar M, Tyszkiewicz T, Wadström T, O’Toole PW. Rapid detection of Helicobacter pylori in gastric biopsy material by polymerase chain reaction. J Clin Microbiol. 1992;30:54-8.
Ahmad N, Zakaria WR, Abdullah SA, Mohamed R. Characterization of clarithromycin resistance in Malaysian isolates of Helicobacter pylori. World J Gastroenterol. 2009;15:3161-5. https://doi.org/10.3748/wjg.15.3161
Yula E, Nagiyev T, Kaya ÖA, Inci M, Çelik MM, Köksal F. Detection of primary clarithromycin resistance of Helicobacter pylori and association between cagA + status and clinical outcome. Folia Microbiol (Praha). 2013;58:141-6. https://doi.org/10.1007/s12223-012-0192-8
Mahmoudi S, Mamishi S, Banar M, Keshavarz Valian S, Bahador A, Najafi M, et al. Antibiotic susceptibility of Helicobacter pylori strains isolated from Iranian children: High frequency of A2143G point mutation associated with clarithromycin resistance. J Glob Antimicrob Resist. 2017;10:131-5. https://doi.org/10.1016/j.jgar.2017.04.011
Abdollahi H, Savari M, Zahedi MJ, Moghadam SD, Abasi MH. Detection of A2142C, A2142G, and A2143G mutations in 23s rRNA gene conferring resistance to clarithromycin among Helicobacter pylori isolates in Kerman, Iran. Iran J Med Sci. 2011;36:104-10.
Pourakbari B, Mahmoudi S, Parhiz J, Sadeghi RH, Monajemzadeh M, Mamishi S. High frequency of metronidazole and clarithromycin-resistant Helicobacter pylori in formalin-fixed, paraffin-embedded gastric biopsies. Br J Biomed Sci. 2018;75:61-5. https://doi.org/10.1080/09674845.2017.1391466
Henao SC, Quiroga A, Martínez JD, Otero W. Resistencia primaria a la claritromicina en aislamientos de Helicobacter pylori. Rev Colomb Gastroenterol. 2009;24:110-4.
Figueroa M, Cortés A, Pazos A, Bravo LE. Susceptibilidad in vitro de Helicobacter pylori a amoxicilina y claritromicina obtenido a partir de biopsias gástricas de pacientes de zona de bajo riesgo para cáncer gástrico. Biomédica. 2012;32:32-42. https://doi.org/10.7705/biomedica.v32i1.454
Yepes CA, Rodríguez A, Ruiz Á, Ariza B. Antibiotics resistance of Helicobacter pylori at the San Ignacio University Hospital in Bogotá. Acta Medica Colomb. 2008;33:11-4.
Álvarez A, Moncayo JI, Santacruz JJ, Corredor LF, Reinosa E, Martínez JW, et al. Resistencia a metronidazol y claritromicina en aislamientos de Helicobacter pylori de pacientes dispépticos en Colombia. Rev Med Chil. 2009;137:1309-14. https://doi.org/10.4067/S0034-98872009001000005
Álvarez A, Moncayo JI, Santacruz JJ, Santacoloma M, Corredor LF, Reinosa E. Antimicrobial susceptibility and mutations involved in clarithromycin resistance in Helicobacter pylori isolates from patients in the western central region of Colombia. Antimicrob Agents Chemother. 2009;53:4022-4. https://doi.org/10.1128/AAC.00145-09
Bustamante-Rengifo JA, Matta AJ, Pazos A, Bravo LE. In vitro effect of amoxicillin and clarithromycin on the 3’ region of cagA gene in Helicobacter pylori isolates. World J Gastroenterol. 2013;19:6044-54. https://doi.org/10.3748/wjg.v19.i36.6044
Sanches BS, Martins GM, Lima K, Cota B, Moretzsohn LD, Ribeiro LT, et al. Detection of Helicobacter pylori resistance to clarithromycin and fluoroquinolones in Brazil: A national survey observational study. World J Gastroenterol. 2016;22:7587-94. https://doi.org/10.3748/wjg.v22.i33.7587
Zerbetto G, Mendiondo N, Wonaga A, Viola L, Ibarra D, Campitelli E, et al. Occurrence of mutations in the antimicrobial target genes related to levofloxacin, clarithromycin, and amoxicillin resistance in Helicobacter pylori isolates from Buenos Aires City. Microb Drug Resist. 2016;23:351-8. https://doi.org/10.1089/mdr.2015.0361
Alarcón-Millán J, Fernández-Tilapa G, Cortés-Malagón EM, Castañón-Sánchez CA, De Sampedro-Reyes J, Cruz-del Carmen I, et al. Clarithromycin resistance and prevalence of Helicobacter pylori virulent genotypes in patients from Southern México with chronic gastritis. Infect Genet Evol. 2016;44:190-8. https://doi.org/10.1016/j.meegid.2016.06.044
Trespalacios-Rangel AA, Otero W, Arévalo-Galvis A, Poutou-Piñales RA, Rimbara E, Graham DY. Surveillance of levofloxacin resistance in Helicobacter pylori isolates in Bogotá-Colombia (2009-2014). PLoS One. 2016;11:e0160007. https://doi.org/10.1371/journal.pone.0160007
Thung I, Aramin H, Vavinskaya V, Gupta S, Park JY, Crowe SE, et al. Review article: The global emergence of Helicobacter pylori antibiotic resistance. Aliment Pharmacol Ther. 2016;43:514-33. https://doi.org/10.1111/apt.13497
Algunos artículos similares:
- Lino E. Torres, Lidice González, Karelia Melián, Jordis Alonso, Arlenis Moreno, Mayrín Hernández, Orlando Reyes, Ludisleydis Bermúdez, Javier Campos, Guillermo Pérez-Pérez, Boris L. Rodríguez, Patrón de los motivos EPIYA de cepas cubanas de Helicobacter pylori positivas para CagA , Biomédica: Vol. 32 Núm. 1 (2012)
- Mercedes Figueroa, Armando Cortés, Álvaro Pazos, Luis Eduardo Bravo, Sensibilidad in vitro a amoxicilina y claritromicina de Helicobacter pylori obtenido de biopsias gástricas de pacientes en zona de bajo riesgo para cáncer gástrico , Biomédica: Vol. 32 Núm. 1 (2012)
- Yeison Harvey Carlosama , Claudia Patricia Acosta , Carlos Hernán Sierra , Carol Yovanna Rosero , Harold Jofre Bolaños, Sistema OLGA (Operative Link on Gastritis Assessment) como marcador para cáncer gástrico y displasia en una población colombiana de alto riesgo: estudio multicéntrico , Biomédica: Vol. 43 Núm. Sp. 3 (2023): Enfermedades crónicas no transmisibles
- Juan Camilo Caguazango, Álvaro Jairo Pazos, Microbiota según la topografía gástrica en pacientes con bajo y con alto riesgo de cáncer gástrico en Nariño, Colombia , Biomédica: Vol. 39 Núm. Supl. 2 (2019): Enfermedades transmisibles en el trópico, agosto
- Claudia Patricia Acosta, Fabián Andrés Hurtado, Alba Alicia Trespalacios, Determinación de mutaciones de un solo nucleótido en el gen 23S rRNA de Helicobacter pylori relacionadas con resistencia a claritromicina en una población del departamento del Cauca, Colombia , Biomédica: Vol. 34 (2014): Abril, Suplemento 1, Resistencia bacteriana
- Ana María Perilla, Camilo González, Sandra Liliana Valderrama, Natasha Vanegas, Bibiana Chavarro, Luis Carlos Triana, José Roberto Támara, Carlos Arturo Álvarez, Neumonía necrosante por Staphylococcus aureus extrahospitalario resistente a la meticilina:reporte de dos casos en Colombia , Biomédica: Vol. 29 Núm. 4 (2009)
- Andrés Javier Quiroga, Antonio Huertas, Alba Lucía Cómbita, María Mercedes Bravo, Variación en el número de repeticiones EPIYA-C en la proteína CagA de aislamientos colombianos de Helicobacter pylori y su capacidad para inducir fenotipo colibrí en células epiteliales gástricas , Biomédica: Vol. 30 Núm. 2 (2010)
- David Felipe Briceño, Adriana Correa, Carlos Valencia, Julián Andrés Torres, Robinson Pacheco, María Camila Montealegre, Diego Ospina, María Virginia Villegas, Grupo de Resistencia Bacteriana Nosocomial, Actualización de la resistencia a antimicrobianos de bacilos Gram negativos aislados en hospitales de nivel III de Colombia: años 2006, 2007 y 2008 , Biomédica: Vol. 30 Núm. 3 (2010)
- Ingrid Yamile Pulido, José Ramón Mantilla, Emilia María Valenzuela, María Teresa Reguero, Elsa Beatriz González, Distribución de genes codificadores de β-lactamasas de espectro extendido en aislamientos de Klebsiella pneumoniae de hospitales de Bogotá, D.C., Colombia , Biomédica: Vol. 31 Núm. 1 (2011)
- Andrés Javier Quiroga, Diana Marcela Cittelly, María Mercedes Bravo, Frecuencia de los genotipos babA2, oipA y cagE de Helicobacter pylori en pacientes colombianos con enfermedades gastroduodenales. , Biomédica: Vol. 25 Núm. 3 (2005)
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























