Primera evidencia de infección por el virus de la coriomeningitis linfocítica (arenavirus) en roedores Mus musculus capturados en la zona urbana del municipio de Sincelejo, Sucre, Colombia
Resumen
Introducción. El virus de la coriomeningitis linfocítica es un arenavirus del Viejo Mundo que se hospeda en el ratón casero (Mus musculus), y puede causar infecciones congénitas, hidrocefalia, coriorretinitis y falla orgánica múltiple en pacientes receptores de trasplantes. En Colombia aún no se ha reportado la enfermedad mediante diagnóstico clínico, pero en estudios serológicos se ha detectado la infección por el virus Pichindé en roedores en los departamentos del Cauca y Valle del Cauca, y por el virus Guanarito, en roedores en Córdoba.
Objetivo. Detectar el virus de la coriomeningitis linfocítica en M. musculus en el municipio de Sincelejo.
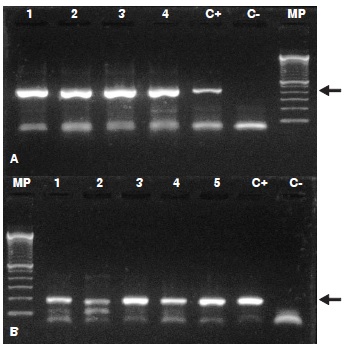
Materiales y métodos. Se evaluaron 80 muestras de plasma mediante la prueba ELISA usando antígeno del virus de la coriomeningitis linfocítica. Además, se empleó la reacción en cadena de la polimerasa con transcriptasa inversa (RT-PCR) anidada en muestras de animales seropositivos y seronegativos para la detección del segmento S.
Resultados. Se encontró una seroprevalencia de 10% (8/80) y se detectó el genoma viral en 16 muestras de cerebro; el alineamiento (en la Basic Local Alignment Search Tool, BLAST) y el análisis filogenético (mediante el programa MrBayes, versión 3.2.2) confirmaron que correspondía al virus de la coriomeningitis linfocítica.
Conclusión. Los resultados indicaron que la infección por el virus de la coriomeningitis linfocítica en humanos podría ocurrir en el área urbana de Sincelejo, aunque hasta la fecha no se hayan reportado casos.
Descargas
Referencias bibliográficas
York J, Berry JD, Stroher U, Li Q, Feldmann H, Lu M, et al. An antibody directed against the fusion peptide of Junin virus envelope glycoprotein GPC inhibits pH-induced membrane fusion. J Virol. 2010;84:6119-29. http://dx.doi.org/10.1128/JVI.02700-09
Machado AM, Figueiredo GG, Campos GM, Lozano ME, Machado AR, Figueiredo LT. Standardization of an ELISA test using a recombinant nucleoprotein from the Junin virus as the antigen and serological screening for arenavirus among the population of Nova Xavantina, State of Mato Grosso. Rev Soc Bras Med Trop. 2010;43:229-33. http://dx.doi.org/10.1590/S0037-86822010000300003
Charrel RN, de Lamballerie X, Emonet S. Phylogeny of the genus Arenavirus. Curr Opin Microbiol. 2008;11:362-8. http://dx.doi.org/10.1016/j.mib.2008.06.001
Charrel RN, de Lamballerie X. Zoonotic aspects of arenavirus infections. Vet Microbiol. 2010;140:213-20. http://dx.doi.org/10.1016/j.vetmic.2009.08.027
Zapata JC, Salvato SM. Arenavirus variations due to hostspecific adaptation. Viruses. 2013;5:241-78. http://dx.doi.org/10.3390/v5010241
Childs JE, Kaufmann AF, Peters CJ, Ehrenberg RL. Hantavirus infection--southwestern United States: Interim recommendations for risk reduction. Centers for Disease Control and Prevention. MMWR Recomm Rep. 1993;42:1-13.
Trapido H, Sanmartín C. Pichindé virus, a new virus of the Tacaribe group from Colombia. Am J Trop Med Hyg. 1971;20:631-41.
Mattar S, Guzmán C, Arrázola J, Soto E, Barrios J, Pini N, et al. Antibody to arenaviruses in rodents, Caribbean Colombia. Emerg Infect Dis. 2011;17:1315-7. http://dx.doi.org/10.3201/eid1707.101961
Arrázola-D J, Londoño A, Arroyabe E, Rodas J, Salazar-Bravo J, Mattar-VS. Vigilancia del virus de la coriomeningitis linfocítica (LCMV) en roedores reservorios de Córdoba (Colombia). Rev Méd Evidencias. 2014;3:5-14.
Mills J, Childs J, Ksiazek T, Peters CJ, Velleca WM. Methods for trapping and sampling small mammals for virologic testing. Atlanta, GA: CDC; 1998.
Nowak R. Walker`s Mammals of the World. Sixth edition. Baltimore: The Johns Hopkins University Press; 1999. p.1-2015.
Ledesma J, Fedele CG, Carro F, Lledó L, Sánchez-Seco MP, Tenorio A, et al. Independent lineage of lymphocytic choriomeningitis virus in wood mice (Apodemus sylvaticus), Spain. Emerg Infect Dis. 2009;15:1677-80. http://dx.doi.org/10.3201/eid1510.090563
Smith LM, Sanders JZ, Kaiser RJ, Hughes P, Dodd C, Connell CR, et al. Fluorescence detection in automated DNA sequence analysis. Nature.1986;321:674-9. http://dx.doi.org/10.1038/321674a0
Sanger F, Nicklen S, Coulson AR. DNA sequencing with chain-terminating inhibitors. Biochemistry. 1977;74:5463-7.
Thompson JD, Higgins DG, Gibson TJ. CLUSTAL W: Improving the sensitivity of progressive multiple sequence alignment through sequence weighting, position-specific gap penalties and weight matrix choice. Nucleic Acids Res. 1994;22:4673-80. http://dx.doi.org/10.1093/nar/22.22.4673
Tamura K, Peterson D, Peterson N, Stecher G, Nei M, Kumar S. MEGA5: Molecular evolutionary genetics analysis using maximum likelihood, evolutionary distance, and maximum parsimony methods. Mol Biol Evol. 2011;28:2731-9. http://dx.doi.org/10.1093/molbev/msr121.
Macneil A, Stroher U, Farnon E, Campbell S, Cannon D, Paddock CD, et al. Solid organ transplant-associated lymphocytic choriomeningitis, United States, 2011. Emerg Infect Dis. 2012;18:1256-62. http://dx.doi.org/10.3201/eid1808.120212
Kallio-Kokko H, Laakkonen J, Rizzoli A, Tagliapietra V, Cattadori I, Perkins SE, et al. Hantavirus and arenavirus antibody prevalence in rodents and humans in Trentino, Northern Italy. Epidemiol Infect. 2006;134:830-6. http://dx.doi.org/10.1017/S0950268805005431
Riera L, Castillo E, Del Carmen-Saavedra M, Priotto J, Sottosanti J, Polop J, et al. Serological study of the lymphochoriomeningitis virus (LCMV) in an inner city of Argentina. J Med Virol. 2005;76:285-9. http://dx.doi.org/10.1002/jmv.20357
Glass GE, Shields T, Cai B, Yates TL, Parmenter R. Persistently highest risk areas for hantavirus pulmonary syndrome: Potential sites for refugia. Ecol Appl. 2007;17:129-39.
Madhav NK, Wagoner KD, Douglass RJ, Mills JN. Delayed density-dependent prevalence of Sin Nombre virus antibody in Montana deer mice (Peromyscus maniculatus) and implications for human disease risk. Vector Borne Zoonotic Dis. 2007;7:353-64. http://dx.doi.org/10.1089/vbz.2006.0605
Lehmer E, Clay C, Pearce-Duvet J, St Jeor S, Dearing M. Differential regulation of pathogens: The role of habitat disturbance in predicting prevalence of Sin Nombre virus. Oecologia. 2008;155:429-39. http://dx.doi.org/10.1007/s00442-007-0922-9
Tersago K, Schreurs A, Linard C, Verhagen R, van Dongen S, Leirs H. Population, environmental, and community effects on local bank vole (Myodes glareolus) Puumala virus infection in an area with low human incidence. Vector Borne Zoonotic Dis. 2008;8:235-44. http://dx.doi.org/10.1089/vbz.2007.0160
Suzan G, Marce E, Giermakowski JT, Armien B, Pascale J, Mills J, et al. The effect of habitat fragmentation and species diversity loss on hantavirus prevalence in Panamá. Ann NY Acad Sci. 2008;1149:80-3. http://dx.doi.org/10.1196/annals.1428.063
Kuenzi AJ, Douglass RJ, Bond CW, Calisher CH, Mills JN. Long-term dynamics of Sin Nombre viral RNA and antibody in deer mice in Montana. J Wildl Dis. 2005;41:473-81. http://dx.doi.org/10.7589/0090-3558-41.3.473
Hjelle B, Glass GE. Outbreak of hantavirus infection in the Four Corners region of the United States in the wake of the 1997-1998 El Niño-southern oscillation. J Infect Dis. 2000;181:1569-73. http://dx.doi.org/1010.1086/315467
Fischer SA, Graham MB, Kuehnert MJ, Kotton CN, Srinivasan A, Marty FM, et al. Transmission of lymphocytic choriomeningitis virus by organ transplantation. N Engl J Med. 2006;354:2235-49. http://dx.doi.org/10.1056/NEJMoa053240
Buchmeier MJ, Peters CJ. Arenaviridae: The viruses and their replication. 5th edition. Philadelphia, PA: Lippincott Williams & Wilkins; 2001. p. 1791-828.
Jamieson D, Bell M, Rasmussen S, Kourtis A. Lymphocytic choriomeningitis virus: An emerging obstetric pathogen? Am J Obstet Gynecol 2006;194:1532-6. http://dx.doi.org/10.1016/j.ajog.2005.11.040
Takagi T, Ohsawa M, Morita C, Sato, H, Ohsawa K. Genomic analysis and pathogenic characteristics of lymphocytic choriomeningitis virus strains isolated in Japan. Comp Med. 2012;62:185-92.
Musser G, Carleton M. Mammal species of the world: A taxonomic and geographic reference: Superfamily Muridae. 3rd edition. Washington, DC: Smithsonian Institution; 2005. p. 894-1531.
Tagliapietra V, Rosa R, Hauffe HC, Laakkonen J, Voutilainen L, Vapalahti O, et al. Spatial and temporal dynamics of lymphocytic choriomeningitis virus in wild rodents, northern Italy. Emerg Infect Dis. 2009;15:1019-25. http://dx.doi.org/10.3201/eid1507.081524
Zinkernagel RM. Immunity, immunopathology and vaccines against HIV? Vaccine. 2002;20:1913-7. http://dx.doi.org/10.1016/S0264-410X(02)00066-X
Peters CJ, Wilson MR. Diseases of the central nervous system caused by lymphocytic choriomeningitis virus and other arenaviruses. Handb Clin Neurol. 2014;123:671-81. http://dx.doi.org/10.1016/B978-0-444-53488-0.00033-X
King CC, Jamieson BD, Reddy K, Bali N, Concepcion RJ, Ahmed R. Viral infection of the thymus. J Virol. 1992;66:3155-60.
Oldstone MB, Frank FJ. Pathogenesis of chronic disease associated with persistent lymphocytic choriomeningitis viral infection. I. Relationship of antibody production to disease in neonatally infected mice. J Exp Med. 1969;129:483-505.
Rodríguez M, Buchmeier MJ, Oldstone MB, Lampert PW. Ultrastructural localization of viral antigens in the CNS of mice persistently infected with lymphocytic choriomeningitis virus (LCMV). Am J Pathol. 1983;110:95-100.
Nathanson N, Ahmed R, Biron C, Briton M, González-Scarano F, Griffin D, et al. Viral pathogenesis and immunity. Second edition. California, USA: Academic Press; p. 2007. p . 265.
Heeney JL. Zoonotic viral diseases and the frontier of early diagnosis, control and prevention. J Intern Med. 2006;260:399-408. http://dx.doi.org/10.1111/j.1365-2796. 2006.01711.x
Mets MB, Barton LL.Congenital lymphocytic choriomeningitis virus infection: Decade of rediscovery. Clin Infect Dis. 2006;33:70-4. http://dx.doi.org/10.1086/321897
Algunos artículos similares:
- Constanza Pardo, Ricardo Cendales, Supervivencia de pacientes con cáncer de cuello uterino tratadas en el Instituto Nacional de Cancerología , Biomédica: Vol. 29 Núm. 3 (2009)
- Concepción Judith Puerta, Paula Ximena Pavia, Marleny Montilla, Carolina Flórez, Giomar Herrera, Juan Manuel Ospina, Fred Manrique, Rubén Santiago Nicholls, Reporte del primer caso de enfermedad de Chagas transplacentaria analizado por AP-PCR en Moniquirá, Boyacá , Biomédica: Vol. 29 Núm. 4 (2009)
- Yolanda Lucía López, Claudia González, Berta Natalia Gallego, Ana Lida Moreno, Rectoría de la vigilancia en salud pública en el sistema de seguridad social en salud de Colombia: estudio de casos , Biomédica: Vol. 29 Núm. 4 (2009)
- Oscar Fernando Herrán, María F. Ardila, Tipología de los consumidores de alcohol y sus factores determinantes en Bucaramanga, Colombia , Biomédica: Vol. 29 Núm. 4 (2009)
- Vanihamín Domínguez, Itzen Aguiñiga, Leticia Moreno, Beatriz Torres, Edelmiro Santiago-Osorio, El caseinato de sodio incrementa número de linfocitos B en ratones , Biomédica: Vol. 37 Núm. 4 (2017)
- Andrés F. Londoño, Silvana Levis, Juan D. Rodas, Hantavirus como agentes emergentes de importancia en Suramérica , Biomédica: Vol. 31 Núm. 3 (2011)
- Berta Nelly Restrepo, Margarita Arboleda, Ruth Ramírez, Gonzalo Álvarez, Actividad sérica de la acetilhidrolasa del factor activador de plaquetas en pacientes afrodescendientes y mestizos con dengue, Colombia , Biomédica: Vol. 31 Núm. 4 (2011)
- Sandy Milena Caldera, María Cristina Jaramillo, Suljey Cochero, Alveiro Pérez-Doria, Eduar Elías Bejarano, Diferencias genéticas entre poblaciones de Aedes aegypti de municipios del norte de Colombia, con baja y alta incidencia de dengue , Biomédica: Vol. 33 (2013): Suplemento 1, Fiebres hemorrágicas
- Mabel Carabalí, Clara Beatriz Ocampo, María Eugenia Toledo, Lyda Osorio, Difusión masiva de reportes situacionales sobre dengue: efectos de la intervención en Guadalajara de Buga, Colombia , Biomédica: Vol. 33 (2013): Suplemento 1, Fiebres hemorrágicas
- Ricardo Cendales, Constanza Pardo, Claudia Uribe, Guillermo López, María Clara Yépez, Luis Eduardo Bravo, Calidad de los datos en los registros de cáncer de base de población en Colombia , Biomédica: Vol. 32 Núm. 4 (2012)
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























