Molecular diagnosis of extrapulmonary tuberculosis and sensitivity to rifampicin with an automated real-time method
Abstract
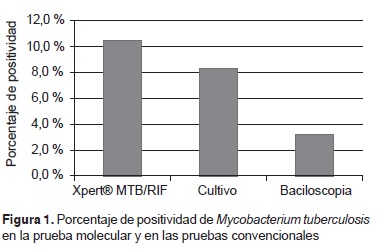
Introduction: Tuberculosis continues to be a global public health problem, the extrapulmonary form being estimated to occur in 10-20% of immunocompetent individuals, increasing in patients who are carriers of the human immunodeficiency virus (HIV); its diagnosis is difficult with conventional methods due to the paucibacillary nature of samples. The Xpert® MTB/RIF test represents an important development in the molecular detection of Mycobacterium tuberculosis and has been used with a variety of non-respiratory clinical samples. Objective: To determine the effectiveness of Xpert® MTB/RIF in the detection of M. tuberculosis and sensitivity to rifampicin in patients with suspected extrapulmonary tuberculosis attending Hospital Universitario de San Vicente Fundación in Medellín in 2013-2014. Materials and methods: This was a descriptive, cross-sectional ambispective study of 372 consecutive samples from 301 patients with suspected extrapulmonary tuberculosis, who were subjected to bacilloscopy, followed by culture in Ogawa Kudoh and the Xpert® MTB/RIF molecular test. Results: The most frequent base diagnosis (60%) for the 182 patients was infection with HIV. Using the culture as reference, the sensitivity and general specificity of the molecular test was 94% (95% CI: 83-100) and 97% (95% CI: 95-99), respectively; for bacilloscopy it was 38.71(95% CI: 19-57) and 100% (95% CI: 99-100), respectively. Sensitivities higher than 75% were found in analyses stratified by samples. Thirty-seven of the isolates were sensitive and one resistant to rifampicin. Conclusion: Xpert® MTB/RIF performed well in samples from different tissues and liquids, representing a significant advance in support of extrapulmonary tuberculosis diagnosis in terms of time and percentage positivity.
Downloads
References
World Health Organization. Twentieth global report on tuberculosis. Report number WHO/HTM/TB/2015.22. Geneva: World Health Organization; 2015. Fecha de consulta: 7 de diciembre de 2015. Disponible en: http://apps.who.int/iris/bitstream/10665/191102/1/9789241565059_eng.pdf.
Instituto Nacional de Salud. Informe final tuberculosis, Colombia, 2014. Fecha de consulta: 1 de diciembre de 2015. Disponible en: http://www.ins.gov.co/lineas-de-accion/Subdireccion-Vigilancia/Informe%20de%20Evento%20Epidemiolgico/Tuberculosis%202014.pdf.
Lado-Lado FL, Prieto-Martínez A, Cabarcos-Ortiz De Barrón A, Carballo-Arceo E, Barrio-Gómez E. Recurrence of tuberculosis in patients infected with the human immunodeficiency virus. An Med Interna. 2001;18:243-7.
Golden MP, Vikram HR. Extrapulmonary tuberculosis: An overview. Am Fam Physician. 2005;72:1761-8.
Raviglione MC, O´Brien R. Mycobacterial diseases. In: Harrison's Principles of Internal Medicine. 18th edition. New York: McGraw-Hill; 2012. p. 1340-59.
Hesselink DA, Yoo SM, Verhoeven GT, Brouwers JW, Smit FJ, van Saase JL. A high prevalence of culture-positive extrapulmonary tuberculosis in a large Dutch teaching hospital. Neth J Med. 2003;61:65-70.
Dye C, Scheele S, Dolin P, Pathania V, Raviglione MC. Consensus statement. Global burden of tuberculosis: Estimated incidence, prevalence, and mortality by country. WHO Global Surveillance and Monitoring Project. JAMA. 1999;282:677-86. http://dx.doi.org/10.1001/jama.282.7.677.
Pacheco M, Awad C, Arias G, Ojeda P, Garay M, Lara A, et al. Extrapulmonary tuberculosis. A perspective from a third-level hospital. Rev Colomb Neumol. 2013;25:16-26.
Canetti G, Rist N, Grosset J. Measurement of sensitivity of the tuberculous bacillus to antibacillary drugs by the method of proportions. Methodology, resistance criteria, results and interpretation. Rev Tuberc Pneumol (Paris). 1963;27:217-72.
Mishra B, Rockey SM, Gupta S, Srinivasa H, Muralidharan S. Multi-drug-resistant tuberculosis: The experience of an urban tertiary care hospital in South India using automated BACTEC 460 TB. Trop Doct. 2012;42:35-7. http://dx.doi.org/10.1258/td.2011.110247.
Skenders GK, Holtz TH, Riekstina V, Leimane V. Implementation of the INNO-LiPA Rif. TB® line-probe assay in rapid detection of multidrug-resistant tuberculosis in Latvia. Int J Tuberc Lung Dis. 2011;15:1546-52. http://dx.doi.org/10.5588/ijtld.11.0067.
Barnard M, Gey van Pittius NC, van Helden PD, Bosman M, Coetzee G, Warren RM. The diagnostic performance of the GenoType MTBDRplus version 2 line probe assay is equivalent to that of the Xpert MTB/RIF assay. J Clin Micro-biol. 2012;50:3712-6. http://dx.doi.org/10.1128/JCM.01958-12.
Bicmen C, Gunduz AT, Coskun M, Senol G, Cirak AK, Ozsoz A. Molecular detection and identification of Mycobacterium tuberculosis complex and four clinically important nontuberculous mycobacterial species in smear-negative clinical samples by the genotype mycobacteria direct test. J Clin Microbiol. 2011;4:2874-8. http://dx.doi.org/10.1128/JCM.00612-11.
Lawn SD, Nicol MP. Xpert® MTB/RIF assay: Development, evaluation and implementation of a new rapid molecular diagnostic for tuberculosis and rifampicin resistance. Future Microbiol. 2011;6:1067-82. http://dx.doi.org/10.2217/fmb.11.84.
Blakemore R, Nabeta P, Davidow AL, Vadwai V, Tahirli R, Munsamy V, et al. A multisite assessment of the quantitative capabilities of the Xpert MTB/RIF assay. Am J Respir Crit Care Med. 2011;184:1076-84. http://dx.doi.org/10.1164/rccm.201103-0536OC.
World Health Organization. Report of the Tenth Meeting WHO Strategic and Technical Advisory Group for Tuberculosis (STAGTB), 27-29 September, 2010. Geneva, World Health Organization; 2010. Fecha de consulta: 30 de noviembre de 2015. Disponible en: http://www.who.int/tb/advisory_bodies/stag_tb_report_2015.pdf?ua=1.
Centers for Disease Control and Prevention. Updated guidelines for the use of nucleic acid amplification tests in the diagnosis of tuberculosis. Morb Mortal Wkly Rep. 2009;58:7-10.
Lawn SD, Zumla AI. Diagnosis of extrapulmonary tuberculosis using the Xpert(®) MTB/RIF assay. Expert Rev Anti Infect Ther. 2012;10:631-5. http://dx.doi.org/10.1586/eri.12.43.
Scott LE, Beylis N, Nicol M, Nkuna G, Molapo S, Berrie L, et al. The diagnostic accuracy of Xpert MTB/RIF on extrapulmonary tuberculosis specimens: Establishing a laboratory testing algorithm for South Africa. J Clin Microbiol. 2014;52:1818-23. http://dx.doi.org/10.1128/JCM.03553-13.
Tortoli E, Russo C, Piersimoni C, Mazzola E, Dal Monte P, Pascarella M, et al. Clinical validation of Xpert MTB/RIF for the diagnosis of extrapulmonary tuberculosis. Eur Respir J. 2012;40:442-7. http://dx.doi.org/10.1183/09031936.00176311.
World Health Organization. Automated real-time nucleic acid amplification technology for rapid and simultaneous detection of tuberculosis and rifampicin resistance. Xpert MTB/RIF assay for the diagnosis of pulmonary and extrapulmonary TB in adults and children: Policy update. Geneva: World Health Organization; 2013. Fecha de consulta: 16 de septiembre de 2015. Disponible en: http://www.ncbi.nlm.nih.gov/books/NBK258608/.
Organización Panamericana de la Salud. Manual para el diagnóstico bacteriológico de la tuberculosis. Parte 2, cultivo. Washington, D.C.: OPS; 2008.
Marín DC, Aristizábal BH. Métodos diagnósticos moleculares en tuberculosis. Med UPB. 2013;32:144-50.
Vadwai V, Boehme CC, Nabeta P. A new pillar in diagnosis of extrapulmonary tuberculosis? Clin Microbiol. 2011;49:2540-5. http://dx.doi.org/10.1128/JCM.02319-10.
Montúfar FE, Aguilar-Londoño C, Saldarriaga-Acevedo C, Quiroga-Echeverri A, Montaño B, et al. Características clínicas, factores de riesgo y perfil de susceptibilidad de las infecciones por micobacterias documentadas por cultivo, en un hospital universitario de alta complejidad en Medellín (Colombia). Rev Chil Infectol. 2014;31:735-42. http://dx.doi.org/10.4067/S0716-10182014000600015.
Centers for Disease Control and Prevention. Guidelines for prevention and treatment of opportunistic infections in HIV-infected adults and adolescents. MMWR Recomm Rep. 2009;58:1-207.
Vittor AY, Garland JM, Gilman RH. Molecular diagnosis of TB in the HIV positive population. Ann Glob Health. 2014; 80:476-85. http://dx.doi.org/10.1016/j.aogh.2015.01.001.
Lawn SD, Brooks SV, Kranzer K, Nicol MP, Whitelaw A, Vogt M, et al. Screening for HIV-associated tuberculosis and rifampicin resistance before antiretroviral therapy using the Xpert MTB/RIF assay: A prospective study. PLoS Med. 2011;8:e1001067. http://dx.doi.org/10.1371/journal.pmed.1001067.
Pérez-Guzmán C, Vargas MH, Arellano-Macías M del R, Hernández-Cobos S, García-Ituarte AZ, Serna-Vela FJ. Clinical and epidemiological features of extrapulmonary tuberculosis in a high incidence region. Salud Pública Mex. 2014;56:189-96.
Hussain SF, Irfan M, Abbasi M, Anwer SS, Davidson S, Haqqee R, et al. Clinical characteristics of 110 miliary tuberculosis patients from a low HIV prevalence country. Int J Tuberc Lung Dis. 2004;8:493-9.
Secretaría de Salud de Medellín. Boletín epidemiológico de Medellín. Alcaldía de Medellín; 2014. Fecha de consulta: 30 de noviembre de 2015. Disponible en: https://www.medellin.gov.co/irj/go/km/docs/pccdesign/SubportaldelCiudadano_2/PlandeDesarrollo_0_19/Publicaciones/Shared%20Content/Boletines/Bolet%C3%ADn%20epidemiol%C3%B3gico%204%20de%202015%20-%20Tuberculosis.pdf.
Clemente M, Palacios J, Penedo A, Álvarez M, Velasco Z, Pando A, et al. Accuracy of the Xpert MTB/RIF test for rapid diagnosis of extrapulmonary tuberculosis. Am J Respir Crit Care Med. 2012;185:A4717. http://dx.doi.org/10.1164/ajrccm-conference.2012.185.1_meetingabstracts.a4717.
Causse M, Ruiz P, Gutiérrez-Aroca JB, Casal M. Comparison of two molecular methods for rapid diagnosis of extrapulmonary tuberculosis. J Clin Microbiol. 2011;49: 3065-7. http://dx.doi.org/10.1128/JCM.00491-11.
Realpe T, Mejía G, Zapata E, Barón P, Gómez V, Robledo J. Evaluación del desempeño de una prueba molecular comercial para el diagnóstico de tuberculosis y la resistencia a rifampicina en muestras clínicas. Hechos Microbiológicos. 2014;5:41.
Moure R, Martín R, Alcaide F. Effectiveness of an integrated real-time PCR method for detection of the Mycobacterium tuberculosis complex in smear-negative extrapulmonary samples in an area of low tuberculosis prevalence. J Clin Microbiol. 2012;50:513-5. http://dx.doi.org/10.1128/JCM.06467-11.
Ferreiro L, San José E, Valdés L. Derrame pleural tuberculoso. Arch Bronconeumol. 2014;50:435-43. http://dx.doi.org/10.1016/j.arbres.2013.07.006.
Porcel JM, Palma R, Valdés L, Bielsa S, San-José E, Esquerda A. Xpert® MTB/RIF in pleural fluid for the diagnosis of tuberculosis. Int J Tuberc Lung Dis. 2013;17:1217-9. http://dx.doi.org/10.5588/ijtld.13.0178.
Friedrich SO, von Groote-Bidlingmaier F, Diacon AH. Xpert MTB/RIF assay for diagnosis of pleural tuberculosis. J Clin Microbiol. 2011;49:4341-2. http://dx.doi.org/10.1128/JCM.05454-11.
Rock RB, Olin M, Baker CA, Molitor TW, Peterson PK. Central nervous system tuberculosis: Pathogenesis and clinical aspects. Clin Microbiol Rev. 2008;21:243-61. http://dx.doi.org/10.1128/CMR.00042-07.
Katti MK. Pathogenesis, diagnosis, treatment, and outcome aspects of cerebral tuberculosis. Med Sci Monit. 2004;10:RA215-29.
Denkinger CM, Schumacher SG, Boehme CC, Dendukuri N, Pai M, Steingart KR. Xpert MTB/RIF assay for the diagnosis of extrapulmonary tuberculosis: A systematic review and meta-analysis. Eur Respir J. 2014;44:435-46. http://dx.doi.org/10.1183/09031936.00007814.
González-Martín J, García-García JM, Anibarro L, Vidal R, Esteban J, Blanquer R, et al. Documento de consenso sobre diagnóstico, tratamiento y prevención de la tuberculosis. Enferm Infecc Microbiol Clin. 2010;28:e1-297-20. http://dx.doi.org/10.1016/j.eimc.2010.02.006.
Agudelo C, Builes L, Hernández M, Robledo J. Nuevos métodos para el diagnóstico del tuberculosis. Iatreia. 2008;21:321-32.
Marlowe EM, Novak-Weekley SM, Cumpio J, Sharp SE, Momeny MA, Babst A, et al. Evaluation of the Cepheid Xpert MTB/RIF assay for direct detection of Mycobacterium tuberculosis complex in respiratory specimens. J Clin Microbiol. 2011;49:1621-3. http://dx.doi.org/10.1128/JCM.02214-10.
Centers for Disease Control and Prevention. Testing for TB infection. 2014. Fecha de consulta: 13 de agosto de 2015. Disponible en: http://www.cdc.gov/tb/topic/testing/default.htm.
Penz E, Boffa J, Roberts DJ, Fisher D, Cooper R, Ronksley PE, et al. Diagnostic accuracy of the Xpert® MTB/RIF assay for extra-pulmonary tuberculosis: A meta-analysis. Int J Tuberc Lung Dis. 2015;19:278-84. http://dx.doi.org/10.5588/ijtld.14.0262.
World Health Organization. Xpert MTB/RIF implementation manual: Technical and operational "how-to"; practical considerations. WHO/HTM/TB/2014.1 Geneva: WHO; 2014. Fecha de consulta: 12 de agosto de 2015. Disponible en: http://who.int/tb/publications/xpert_implem_manual/en/.
Ajantha GS, Shetty PC, Kulkarni RD, Biradar U. PCR as a diagnostic tool for extra-pulmonary tuberculosis. J Clin Diagn Res. 2013;7:1012-5. http://dx.doi.org/10.7860/JCDR/2013/5425.3075.
World Health Organization. The Global Plan to Stop TB, 2006-2015. Fecha de consulta: 10 de julio de 2013. Disponible en: http://www.who.int/tb/publications/2006/en/.
Some similar items:
- Juan Gabriel Bueno-Sánchez, Jairo René Martínez-Morales, Elena E. Stashenko, Wellman Ribón, Anti-tubercular activity of eleven aromatic and medicinal plants occurring in Colombia , Biomedica: Vol. 29 No. 1 (2009)
- María Consuelo Garzón, Dailyn Yorledy Angée, Claudia Llerena, Dora Leticia Orjuela, Jorge Ernesto Victoria, Surveillance of Mycobacterium tuberculosis resistance to antituberculosis drugs , Biomedica: Vol. 28 No. 3 (2008)
- Wellman Ribón, Claudia Castro, Liliana González, Juan Carlos Rozo, Gloria Puerto, Biosafety evaluation of the DNA extraction protocol for Mycobacterium tuberculosis complex species, as implemented at the Instituto Nacional de Salud, Colombia , Biomedica: Vol. 29 No. 4 (2009)
- Leandro Galvis, Ángel Y. Sánchez, Leonardo F. Jurado, Martha I. Murcia, Tuberculosis associated with tumor necrosis factor-α antagonists, case description and analysis of reported cases in Colombia , Biomedica: Vol. 38 No. 1 (2018)
- Diego Chaves, Andrea Sandoval, Luis Rodríguez, Juan C. García, Silvia Restrepo, María Mercedes Zambrano, Comparative analysis of six Mycobacterium tuberculosis complex genomes , Biomedica: Vol. 30 No. 1 (2010)
- Flor de María Cáceres, Luis Carlos Orozco, Incidence of and factors for non-compliance to antituberculous treatment , Biomedica: Vol. 27 No. 4 (2007)
- Diana Castaño, Mauricio Rojas, Alterations in recruitment and activation of Rab proteins during mycobacterial infection , Biomedica: Vol. 30 No. 2 (2010)
- Claudia Llerena, Santiago Elías Fadul, María Consuelo Garzón, Graciela Mejía, Dora Leticia Orjuela, Luz Mary García, Hilda Beatriz Álvarez, Fernando Javier Ruiz, Drug-resistant Mycobacterium tuberculosis in children under 15 years , Biomedica: Vol. 30 No. 3 (2010)
- Constanza Collazos, Gabriel Carrasquilla, Milcíades Ibáñez, Lilia Edith López, Prevalence of respiratory symptomatic in health institutions of Bogotá, Colombia , Biomedica: Vol. 30 No. 4 (2010)
- Marcela López, Claudia Álvarez, Utility of nitrate reductase assay for detection of multidrug-resistant Mycobacterium tuberculosis in a low resource setting , Biomedica: Vol. 31 No. 2 (2011)
| Article metrics | |
|---|---|
| Abstract views | |
| Galley vies | |
| PDF Views | |
| HTML views | |
| Other views | |