Budget impact analysis of primary screening with the HPV test and genotyping against conventional cytology in Colombia
Abstract
Introduction: The detection of the human papillomavirus (HPV) through the combination of the HPV test and other techniques such as cytology has impacted the detection and timely treatment of lesions associated with cervical cancer.
Objective: To estimate the budgetary impact of the strategy of early detection of HPV with DNA test genotyping with reflex cytology versus conventional cytology in women aged 30 to 65 years attending the cervical cancer screening program at a health benefit managing entity in Colombia.
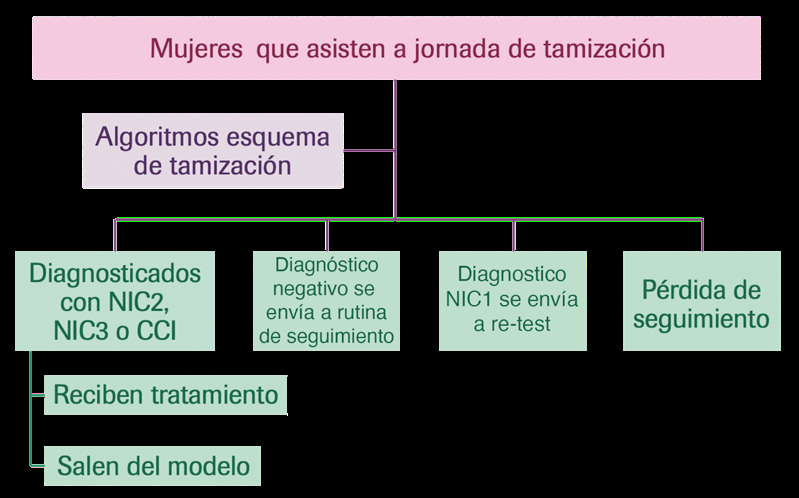
Materials and methods: Using a decision tree and a Markov model, the clinical implications and direct costs of screening, diagnosis, and treatment were estimated in a cohort of women. The analysis considered two screening cycles and their annual costs. The data on the prevalence of clinical results and the costs were taken from the health managing entity. The information on the progression, persistence, and regression of the health states were taken from the ATHENA study.
Results: The screening scheme with the HPV test, genotyping, and reflex cytology compared to conventional cytology was cost-saving. The average cost per screening cycle with the HPV test was estimated at COP $ 129,201,363 and with cytology at COP $ 186,309,952, i.e., a saving of COP $ 57,108,589 (30.7%).
Conclusion: The implementation of the screening strategy under evaluation suggests prospective savings derived from the early detection of health states associated with the development of cervical cancer.
Downloads
References
The American Cancer Society. Prueba de VPH ADN. Fecha de consulta: 1 de julio 2018. Disponible en: https://www.cancer.org/es/cancer/cancer-de-cuello-uterino/detecciondiagnostico-clasificacion-por-etapas/pruebas-de-deteccion/prueba-de-vph.html
Ministerio de Salud y Protección Social. Guía de práctica clínica para la detección y manejo de lesiones precancerosas de cuello uterino. Guía para pacientes y cuidadores. Colombia 2014. Fecha de consulta: 28 de agosto de 2018. Disponible en: https://www.minsalud.gov.co/sites/rid/Lists/BibliotecaDigital/RIDE/DE/CA/gpc-lesiones-precancerosas-cuello-uterinopadres.pdf
Bray F, Ferlay J, Soerjomataram I, Siegel RL, Torre LA, Jemal A. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2018;68:394-424. https://doi.org/10.3322/caac.21492
Martínez-Gómez VM, Martínez JC. Protocolo de vigilancia en salud pública de cáncer de mama y cuello uterino. Bogotá, D.C.: Instituto Nacional de Salud; 2017. p. 1-19.
Saslow D, Solomon D, Lawson HW, Killackey M, Kulasingam SL, Cain J, et al. American Cancer Society, American Society for Colposcopy and Cervical Pathology, and American Society for Clinical Pathology screening guidelines for the prevention and early detection of cervical cancer. CA Cancer J Clin. 2012;62:147-72. https://doi.org/10.3322/caac.21139
Cuenta de Alto Costo. Indicadores prioritarios para la medición, evaluación y monitoreo de la gestión de riesgo por parte de aseguradores y prestadores en pacientes con cáncer de mama y cuello uterino en Colombia. Bogotá, D.C.: Cuenta de Alto Costo; 2016. p. 1-118.
Rincón-Martínez LM, García-Peralta DM. Las pruebas de ADN para el virus papiloma humano -VPH-. Hechos & Acciones. 2012;4:1-8.
Heideman DAM, Hesselink AT, Berkhof J, van Kemenade F, Melchers WJG, Fransen-Daalmeijer N, et al. Clinical validation of the cobas 4800 HPV test for cervical screening purposes. J Clin Microbiol. 2011;49:3983-5. https://doi.org/10.1128/JCM.05552-11
Roche Molecular Systems Inc. Prueba cobas® VPH. Cobas®. 2016. Fecha de consulta: 28 de agosto de 2018. Disponible en: https://spanish.VPH16and18.com/hcp/prueba-cobas-VPH/confiabilidadcon-la-prueba-cobas-VPH.html
Instituto Nacional de Cancerología. Recomendaciones para la tamización de neoplasias del cuello uterino en mujeres sin antecedentes de patología cervical (preinvasora o invasora) en Colombia. Bogotá: INC; 2007. p. 64. Fecha de consulta: 28 de agosto de 2018. Disponible en: https://www.minsalud.gov.co/sites/rid/Lists/BibliotecaDigital/RIDE/IA/INCA/Guia-tamizacioncuello-uterino.pdf
Rincón-Martínez LM, García-Peralta DM. Las pruebas de ADN para el virus papiloma humano -VPH-. Los nuevos retos en la tamización para cáncer de cuello uterino. Bogotá: Instituto Nacional de Cancerología; 2012. Fecha de consulta: 28 de agosto de 2018. Disponible en: http://www.cancer.gov.co/files/libros/archivos/354cd559443a595ea80d9dd1b968974e_Hechos%20y%20Acciones%20VIA%20VILI.pdf
Wright TC, Stoller MH, Behrens CM, Apple R, Darion T, Wright TL. The ATHENA human papillomavirus study: Design, methods, and baseline results. Am J Obstet Gynecol. 2012;206:46.e1-11. https://doi.org/10.1016/j.ajog.2011.07.024
Ministerio de Salud y Protección Social. Resolución No. 3280 de 2018. Por medio de la cual se adoptan los lineamientos técnicos y operativos de la ruta integral de atención para la promoción y mantenimiento de la salud y la ruta integral de atención en salud para la población materno perinatal y se establecen las directrices para su operación. Bogotá, D.C.: Minsalud; 2018. p. 348.
Ministerio de Salud y Protección Social. Lineamientos técnicos y operativos para la vacunación contra el virus del papiloma humano (VPH). Guía de práctica clínica para la detección y manejo de lesiones precancerosas de cuello uterino. Guía para pacientes y cuidadores. Bogotá, D.C.: Minsalud; 2012.
Colín MC, Domínguez MV, Mendieta H, Rojas IJ, Romero MS. Sensibilidad y especificidad de las pruebas de citología, colposcopia, biopsia y detección del virus del papiloma humano en lesión intraepitelial escamosa. En: Ramírez N, Domínguez MV, editoras. Temas selectos de biomedicina en ciencias de la salud. México: UAEM/EON; 2017. p.153-62.
Wright T, Huang J, Baker E, Garfield S, Hertz D, Cox JT. The budget impact of cervical cancer screening using HPV primary screening. Am J Manag Care. 2016;22:e95-105.
Karl A, Petry U, Barth C. A model to evaluate the costs and clinical effectiveness of human papilloma virus screening compared with annual papanicolaou cytology in Germany. Eur J Obstet Gynecol. 2017;212:132-9. https://doi.org/10.1016/j.ejogrb.2017.03.029
Tjalma WAA, Kim E, Vandeweyer K. The impact on women’s health and the cervical cancerscreening budget of primary HPV screening with dual-stain cytology triage in Belgium. Eur J Obstet Gynecol. 2017;212:171-81. https://doi.org/10.1016/j.ejogrb.2017.01.010
Gamboa O, Chicaíza L, García M, Díaz J, González M, Murillo R, et al. Cost-effectiveness of conventional cytology and HPV DNA testing for cervical cancer screening in Colombia. Salud Pública Méx. 2008;50:276-85.
Some similar items:
- Raúl Murillo, Ricardo Cendales, Carolina Wiesner, Marion Piñeros, Sandra Tovar, Effectiveness of cytology-based cervical cancer screening in the Colombian health system , Biomedica: Vol. 29 No. 3 (2009)
- Ricardo Cendales, Carolina Wiesner, Raúl Hernando Murillo, Marion Piñeros, Sandra Tovar, Juan Carlos Mejía, Quality of vaginal smear for cervical cancer screening: a concordance study , Biomedica: Vol. 30 No. 1 (2010)
- Constanza Pardo, Ricardo Cendales, Survival analysis of cervical cancer patients , Biomedica: Vol. 29 No. 3 (2009)
- Sandra Lorena Girón, Julio César Mateus, Fabián Méndez, Impact of an open waste disposal site on the occurrence of respiratory symptoms and on health care costs of children , Biomedica: Vol. 29 No. 3 (2009)
- Narda María Olarte, Ismael Alberto Valderrama, Karlo Roberto Reyes, Martha Isabel Garzón, Javier Antonio Escobar, Betsy Esperanza Castro, Natasha Vanegas, Methicillin-resistant Staphylococcus aureus colonization in a Colombian hospital intensive care unit: phenotypic and molecular characterization , Biomedica: Vol. 30 No. 3 (2010)
- Adalberto Campo, Luis Alfonso Díaz, Germán Eduardo Rueda, Validity of the brief Zung's scale for screening major depressive episode among the general population from Bucaramanga, Colombia , Biomedica: Vol. 26 No. 3 (2006)
- Claudia Calderón, Rodolfo Dennis, Economic cost of Streptococcus pneumoniae community-acquired pneumonia, meningitis and bacteremia in an adult population that required hospitalization in Bogotá, Colombia , Biomedica: Vol. 34 No. 1 (2014)
- Liliana I. Barrero, Juan S. Castillo, Aura L. Leal, Ricardo Sánchez, Jorge A. Cortés, Carlos A. Álvarez, Andrés L. González, Economic burden of methicillin-resistant Staphylococcus aureus bacteremia in critical care patients in hospitals in Bogotá , Biomedica: Vol. 34 No. 3 (2014)
- Luz Helena Cano, María Natalia Acosta, Adriana Pulido, Adaptation to Spanish and criterion validity of a scale for the screening of emotional and behavioral problems in early childhood , Biomedica: Vol. 38 No. Sup.1 (2018): Suplemento 1, Enfermedades crónicas
- Carlos Andrés Vargas-Alzate, Luis Felipe Higuita-Gutiérrez, Judy Natalia Jiménez-Quiceno, Direct medical costs of urinary tract infections by Gram-negative bacilli resistant to beta-lactams in a tertiary care hospital in Medellín, Colombia , Biomedica: Vol. 39 No. Sp. 1 (2019): Suplemento 1, Microbiología médica, mayo
Funding data
| Article metrics | |
|---|---|
| Abstract views | |
| Galley vies | |
| PDF Views | |
| HTML views | |
| Other views | |