Efecto de la inmunoterapia con alérgenos específicos en pacientes pediátricos con asma atendidos en una institución de salud de Colombia
Resumen
Introducción. El asma es una enfermedad crónica y potencialmente grave. El 80 % de los casos es de origen alérgico, por lo cual la inmunoterapia específica con alérgenos es una alternativa terapéutica que modula el curso natural de la enfermedad.
Objetivo. Evaluar el impacto de la inmunoterapia en pacientes pediátricos con asma atendidos en una institución de salud de Colombia.
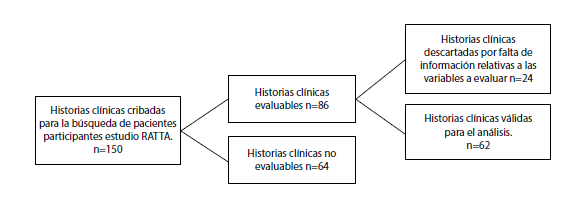
Materiales y métodos. Se hizo un estudio observacional descriptivo con componente analítico de corte transversal. Se incluyeron 62 pacientes con diagnóstico de asma alérgica sensibilizados a ácaros del polvo y en tratamiento, mínimo, con seis dosis de inmunoterapia contra ácaros. El efecto del tratamiento se evaluó mediante la escala de puntuación del ACT (Asthma Control Test), la escala de tratamiento de la GINA (Global Initiative for Asthma) y la espirometría.
Resultados. La puntuación de la prueba ACT antes del inicio de la inmunoterapia, correspondía a 30 % de pacientes con asma no controlada, 28 % con buen control y 4 % con asma totalmente controlada. Entre los pacientes con asma no controlada, el 46,7 % logró un buen control y el 23,3 % alcanzó un control total. En cuanto a la percepción de los pacientes sobre la mejoría con la inmunoterapia, el 9,75 % percibió una mejoría menor del 50 %, el 45,2 %, una entre el 50 y el 90 %, en tanto que el 41,9 % refirió una igual o mayor del 90 %. No se encontraron cambios significativos en los valores del volumen espiratorio forzado en un segundo (VEF1) en las espirometrías.
Conclusiones. Se observaron cambios significativos en los puntajes del ACT y en la percepción de mejoría de la enfermedad en la población tratada con inmunoterapia específica para ácaros, es decir, que esta tendría un efecto beneficioso en el curso natural de la enfermedad.
Descargas
Referencias bibliográficas
Russell RJ, Brightling C. Pathogenesis of asthma: Implications for precision medicine. Clin Sci. 2017;131:1723-35. https://doi.org/10.1042/CS20160253
Dennis R, Caraballo L, García E, Caballero A, Aristizábal G, Córdoba H, et al. Asthma and other allergic conditions in Colombia: A study in 6 cities. Ann Allergy Asthma Immunol. 2004;93:568-74. https://doi.org/10.1016/S1081-1206(10)61265-3
Dennis RJ, Caraballo L, García E, Rojas MX, Rondón MA, Pérez A, et al. Prevalence of asthma and other allergic conditions in Colombia 2009-2010: A cross-sectional study. BMC Pulm Med. 2012;12:17. https://doi.org/10.1186/1471-2466-12-17
Global Initiative for Asthma. Pocket guide for asthma management: For adults and children over 5 years. GINA; 2019. Fecha de consulta: 26 de noviembre de 2019. Disponible en: https://ginasthma.org/wp-content/uploads/2019/04/GINA-2019-main-Pocket-Guide-wms.pdf
Bousquet J, Mantzouranis E, Cruz AA, Aït-Khaled N, Baena-Cagnani CE, Bleecker ER, et al. Uniform definition of asthma severity, control, and exacerbations: Document presented for the World Health Organization Consultation on Severe Asthma. J Allergy Clin Immunol. 2010;126:926-38. https://doi.org/10.1016/j.jaci.2010.07.019
Tran TN, Zeiger RS, Peters SP, Colice G, Newbold P, Goldman M, et al. Overlap of atopic, eosinophilic, and TH2-high asthma phenotypes in a general population with current asthma. Ann Allergy Asthma Immunol. 2016;116:37-42. https://doi.org/10.1016/j.anai.2015.10.027
Lötvall J, Akdis CA, Bacharier LB, Bjermer L, Casale TB, Custovic A, et al. Asthma endotypes: A new approach to classification of disease entities within the asthma syndrome. J Allergy Clin Immunol. 2011;127:355-60. https://doi.org/10.1016/j.jaci.2010.11.037
Posa D, Perna S, Resch Y, Lupinek C, Panetta V, Hofmaier S, et al. Evolution and predictive value of IgE responses toward a comprehensive panel of house dust mite allergens during the first 2 decades of life. J Allergy Clin Immunol. 2017;139: 541-9.e8. https://doi.org/10.1016/j.jaci.2016.08.014
Durham SR. Allergen immunotherapy: 100 years on. Clin Exp Allergy. 2011;41:1171. https://doi.org/10.1111/j.1365-2222.2009.03843.x
Yepes-Núñez JJ, Gómez C, Espinoza Y, Cardona R. Impacto de la inmunoterapia subcutánea con Dermatophagoides farinae y Dermatophagoides pteronyssinus sobre la calidad de vida de pacientes con rinitis y asma alérgica. Biomédica. 2014;34:282-90. https://doi.org/10.7705/biomedica.v34i2.1744
Gaviria R, Ocampo J, Londoño J, Calvo V, Cardona R, Sánchez J. Sensibilización IgE y las condiciones sociodemográficas como determinantes en la gravedad del asma. Revista Alergia México. 2017;64:439. https://doi.org/10.29262/ram.v64i4.291
Rothman KJ, Gallacher JE, Hatch EE. Why representativeness should be avoided. Int J Epidemiol. 2013;42:1012-4. https://doi.org/10.1093/ije/dys223
Schatz M, Sorkness CA, Li JT, Marcus P, Murray JJ, Nathan RA, et al. Asthma Control Test: Reliability, validity, and responsiveness in patients not previously followed by asthma specialists. J Allergy Clin Immunol. 2006;117:549-56. https://doi.org/10.1016/j.jaci.2006.01.011
Bousquet J, Khaltaev N, Cruz AA, Denburg J, Fokkens WJ, Togias A, et al. Allergic Rhinitis and its Impact on Asthma (ARIA) 2008 update (in collaboration with the World Health Organization, GA(2)LEN and AllerGen). Allergy. 2008;63(Suppl.86):8-160. https://doi.org/10.1111/j.1398-9995.2007.01620.x
Roberts G, Pfaar O, Akdis CA, Ansotegui IJ, Durham SR, Gerth van Wijk R, et al. EAACI Guidelines on Allergen Immunotherapy: Allergic rhinoconjunctivitis. Allergy. 2018;73:765-98. https://doi.org/10.1111/all.13317
Gandhi VD, Davidson C, Asaduzzaman M, Nahirney D, Vliagoftis H. House dust mite interactions with airway epithelium: Role in allergic airway inflammation. Curr Allergy Asthma Rep. 2013;13:262-70. https://doi.org/10.1007/s11882-013-0349-9
Abramson MJ, Puy RM, Weiner JM. Injection allergen immunotherapy for asthma. Cochrane Database Syst Rev. 2010. Cochrane Database Syst Rev. 2010;CD001186. https://doi.org/10.1002/14651858.cd001186.pub2
Dhami S, Kakourou A, Asamoah F, Agache I, Lau S, Jutel M, et al. Allergen immunotherapy for allergic asthma: A systematic review and meta-analysis. Allergy. 2017;72:1825-48. https://doi.org/10.1111/all.13208
Acevedo N, Zakzuk J, Caraballo L. House dust mite allergy under changing environments. Allergy Asthma Immunol Res. 2019;11:450-69. https://doi.org/10.4168/aair.2019.11.4.450
Sánchez-Caraballo J, Diez-Zuluaga S, Cardona-Villa R. Sensitization to aeroallergens in allergic patients from Medellín, Colombia. Rev Alerg Mex. 2012;59:139-47.
Fernández-Caldas E, Puerta L, Mercado D, Lockey RF, Caraballo LR. Mite fauna, Der pI, Der f I and Blomia tropicalis allergen levels in a tropical environment. Clin Exp Allergy. 1993;23:292-7. https://doi.org/10.1111/j.1365-2222.1993.tb00325.x
Algunos artículos similares:
- Juan José Yepes-Núñez, Carolina Gómez, Yeinis Espinoza, Ricardo Cardona, Impacto de la inmunoterapia subcutánea con Dermatophagoides farinae y Dermatophagoides pteronyssinus sobre la calidad de vida de pacientes con rinitis y asma alérgica , Biomédica: Vol. 34 Núm. 2 (2014)
- Jorge Sánchez, Ricardo Cardona, Luis Caraballo, Carlos Serrano, Ruth Ramírez, Susana Díez, Elizabeth García, Ana María Segura, Alfonso Cepeda, María Minotas, Inmunoterapia con alérgenos: mecanismos de acción, impacto terapéutico y socioeconómico. Consenso de la Asociación Colombiana de Alergias, Asma e Inmunología , Biomédica: Vol. 36 Núm. 3 (2016)
- Lizeth Huanca-Laura , Marilyn Aparicio , Demetrio Jemio , Mariana Hurtado, Mayra Huanca, Alexis Chuquimia, Relación entre la calidad del aire y el asma en habitantes de grandes altitudes, La Paz, Bolivia (3.600 m.s.n.m.) , Biomédica: Vol. 44 Núm. 2 (2024)
- Ricardo Cardona, Ruth Helena Ramírez, Zulma Reina, Mauricio Fernando Escobar, Edison Morales, Alergia e intolerancia a antiinflamatorios no esteroides: desensibilización exitosa en tres casos y revisión de la literatura , Biomédica: Vol. 29 Núm. 2 (2009)
- Juan Carlos Hernández, Carlos Julio Montoya, Silvio Urcuqui-Inchima, Papel de los receptores tipo toll en las infecciones virales: el VIH-1 como modelo , Biomédica: Vol. 27 Núm. 2 (2007)
- José Fernando Cantillo, Leonardo Puerta, Nuevos esquemas de inmunoterapia específicas con alérgenos , Biomédica: Vol. 30 Núm. 3 (2010)
- Ana M. Aristizábal , Lina P. Montaña , Jaiber Gutiérrez, Diego Medina, Alexis A. Franco , Eliana Manzi , Ángela Devia Zapata , Walter Mosquera , Esteroides intramesentéricos para la enfermedad del injerto contra el huésped resistente a los esteroides en pacientes pediátricos: Una opción segura , Biomédica: Vol. 44 Núm. Sp. 2 (2024): Inmunología clínica, publicación anticipada
- Ángela M. Pedraza, Carlos E. Rodríguez-Martínez, Ranniery Acuña, Validación inicial de una escala para medir el nivel de sobrecarga de padres o cuidadores de niños asmáticos , Biomédica: Vol. 33 Núm. 3 (2013)
- Marcela González, Claudia Patricia González, Alvaro Sanabria, Determinación ecográfica del volumen normal de la glándula tiroides en una población pediátrica de Bogotá, Colombia. , Biomédica: Vol. 26 Núm. 1 (2006)
- Jorge Sánchez, María Nelly Restrepo, José Mopan, Carlos Chinchilla, Ricardo Cardona, Alergia a la leche y al huevo: diagnóstico, manejo e implicaciones en América Latina , Biomédica: Vol. 34 Núm. 1 (2014)
Datos de los fondos
-
Universidad de Antioquia
Números de la subvención 20730003
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























