El caseinato de sodio incrementa número de linfocitos B en ratones
Resumen
Introducción. El caseinato de sodio, una sal de la caseína utilizada como agente proinflamatorio en ratones, es capaz de inducir granulopoyesis en vivo e incrementar la producción de citocinas esenciales en dicho evento.
Objetivo. Evaluar si el caseinato de sodio es capaz de inducir un efecto biológico en células de origen linfoide y la producción de citocinas involucradas con este linaje.
Materiales y métodos: Se utilizaron ratones hembra BALB/c de 8 a 12 semanas de edad. Los animales se inyectaron cuatro veces, con intervalos de 48 horas, por vía intraperitoneal con 1 ml de caseinato de sodio (10 % de SFB p/v). La población de linfocitos B y la incorporación de bromodesoxiuridina (BrdU) se analizaron mediante citometría de flujo. La detección de la interleucina 7 se evaluó mediante la técnica de ELISA.
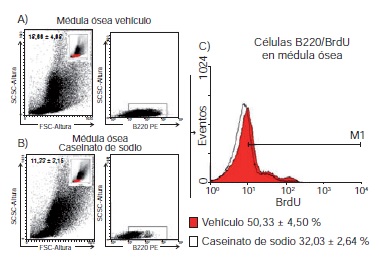
Resultados. Tras la inyección por vía intraperitoneal, el número de linfocitos B 220+ provenientes del bazo de ratones tratados con caseinato de sodio aumentó comparados con los que solo recibieron el vehículo como tratamiento (89,01±1,03 Vs. 75,66±2,08), así como la incorporación de BrdU en células B220+ (38,59±4,48 Vs. 11,82±1,04). Se evidenció, asimismo, el incremento en la concentración de la interleucina 7 (IL-7) en el suero de los ratones tratados con caseinato de sodio, comparados con los que solo recibieron el vehículo (62,1±17,5 Vs. 26,9±4,4 pg/ml).
Conclusión. El caseinato de sodio fue capaz de aumentar el número de linfocitos B en bazo de ratones, así como inducir la producción de IL-7, citocina clave para la linfopoyesis B.
Descargas
Referencias bibliográficas
Lotem J, Sachs L. Control of in vivo differentiation of myeloid leukemic cells. Leukemia. 1988;2:24s-37s.
Lotem J, Sachs L. Independent regulation of myeloid cell growth and differentiation inducing proteins: In vivo regulation by compounds that induce inflammation. Int J Cancer. 1985;35:93-100.
Santiago-Osorio E, Mora L, Bautista M, Montesinos JJ, Martínez I, Ramos-Mandujano G, et al. Sodium caseinate induces secretion of macrophage colony-stimulating factor from neutrophils. Immunobiology. 2010;215:332-9. https://doi.org/10.1016/j.imbio.2009.03.003
Córdova-Galaviz Y, Ledesma-Martínez E, Aguíñiga-Sánchez I, Soldevila-Melgarejo G, Soto-Cruz I, Weiss-Steider B, et al. Sodium caseinate induces increased survival in leukaemic mouse J774 model. In Vivo. 2014;28: 819-25.
Santiago-Osorio E, Ledesma-Martínez E, Aguiñiga-Sánchez I, Poblano-Pérez I, Weiss-Steider B, Montesinos-Montesinos JJ, et al. Sodium caseinate (CasNa) induces mobilization of hematopoietic stem cells in a BALB/c mouse model. Med Sci Monit Basic Res. 2015;21:206-12. https://doi.org/10.12659/MSMBR.895442
Domínguez-Meléndez V, Silvestre-Santana O, Moreno-Fierros L, Aguiñiga-Sánchez I, Martínez L, Marroquín-Segura R, et al. Sodium caseinate induces mouse granulopoiesis. Inflamm Res. 2012;61:367-73. https://doi.org/10.1007/s00011-011-0421-7
Metcalf D, Robb L, Dunn AR, Mifsud S, Di Rago L. Role of granulocyte-macrophage colony-stimulating factor and granulocyte colony stimulating factor in the development of an acute neutrophil inflammatory response in mice. Blood. 1996;88:3755-64.
Wong CW, Seow HF, Liu AH, Husband AJ, Smithers GW, Watson DL. Modulation of immune responses by bovine beta-casein. Immunol Cell Biol. 1996;74:323-9. https://doi.org/10.1038/icb.1996.58
Tobita K, Kawahara T, Otani H. Bovine beta-casein (1-28), a casein phosphopeptide, enhances proliferation and IL-6 expression of mouse CD19+ cells via Toll-like receptor 4. J Agric Food Chem. 2006;54:8013-7. https://doi.org/10.1021/jf0610864
Ma A, Koka R, Burkett P. Diverse functions of IL-2, IL-15, and IL-7 in lymphoid homeostasis. Annu Rev Immunol. 2006;24:657-79. https://doi.org/10.1146/annurev.immunol.24.021605.090727
Sitnicka E, Bryder D, Theilgaard-Mönch K, Buza-Vidas N, Adolfsson J, Jacobsen SE. Key role of flt3 ligand in regulation of the common lymphoid progenitor but not in maintenance of the hematopoietic stem cell pool. Immunity. 2002;17:463-72. https://doi.org/10.1016/S1074-7613(02)00419-3
Peschon JJ, Morrissey PJ, Grabstein KH, Ramsdell FJ, Maraskovsky E, Gliniak BC, et al. Early lymphocyte expansion is severely impaired in interleukin 7 receptor-deficient mice. J Exp Med. 1994;180:1955-60. https://doi.org/10.1084/jem.180.5.1955
Instituto de Biotecnología, Universidad Nacional Autónoma de México. Norma Oficial Mexicana NOM-062-ZOO-1999. Especificaciones técnicas para la producción, cuidado y uso de los animales de laboratorio. Fecha de consulta: 15 de enero de 2010. Disponible en: http://www.ibt.unam.mx/computo/pdfs/bioterio.NOM-062.pdf
Bertrand JY, Giroux S, Golub R, Klaine M, Jalil A, Boucontet L, et al. Characterization of purified intra-embryonic hematopoietic stem cells as a tool to define their site of origin. Proc Natl Acad Sci USA. 2005;102:134-9. https://doi.org/10.1073/pnas.0402270102
Cyster JG. Chemokines, sphingosine-1-phosphate, and cell migration in secondary lymphoid organs. Annu Rev Immunol. 2005;23:127-59. https://doi.org/10.1146/annurev.immunol.23.021704.115628
Fu YX, Chaplin DD. Development and maturation of secondary lymphoid tissues. Annu Rev Immunol. 1999;17: 399-433. https://doi.org/10.1146/annurev.immunol.17.1.399
Dias S, Silva H Jr, Cumano A, Vieira P. Interleukin-7 is necessary to maintain the B cell potential in common lymphoid progenitors. J Exp Med. 2005;201:971-9. https://doi.org/10.1084/jem.20042393
Milne CD, Paige CJ. IL-7: A key regulator of B lympho-poiesis. Semin Immunol. 2006;18:20-30. https://doi.org/10. 1016/j.smim.2005.10.003
Ueda Y, Yang K, Foster SJ, Kondo M, Kelsoe G. Inflam-mation controls B lymphopoiesis by regulating chemokine CXCL12 expression. J Exp Med. 2004;199:47-58. https://doi.org/10.1084/jem.20031104
Ueda Y, Kondo M, Kelsoe G. Inflammation and the reciprocal production of granulocytes and lymphocytes in bone marrow. J Exp Med. 2005;201:1771-80. https://doi.org/10.1084/jem.20041419
von Freeden-Jeffry U, Vieira P, Lucian LA, McNeil T, Burdach SE, Murray R. Lymphopenia in interleukin (IL)-7 gene-deleted mice identifies IL-7 as a nonredundant cytokine. J Exp Med. 1995;181:1519-26. https://doi.org/10. 1084/jem.181.4.1519
Morrison SJ, Wright DE, Weissman IL. Cyclophosphamide/granulocyte colony-stimulating factor induces hematopoietic stem cells to proliferate prior to mobilization. Proc Natl Acad Sci USA. 1997;94:1908-13
Inra CN, Zhou BO, Acar M, Murphy MM, Richardson J, Zhao Z, et al. A perisinusoidal niche for extramedullary haematopoiesis in the spleen. Nature. 2015;26:466-71. https://doi.org/10.1038/nature15530
Algunos artículos similares:
- Alejandra Catalina Vélez, Diana María Castaño, Rubén Darío Gómez, Julio César Orrego, Marcela Moncada, José Luis Franco, Inmunodeficiencia común variable: caracterización clínica e inmunológica de pacientes e identificación de subgrupos homogéneos con base en la tipificación de subpoblaciones de linfocitos B , Biomédica: Vol. 35 Núm. 1 (2015)
- Luis A. Franco, Germán E. Matiz, Jairo Calle, Roberto Pinzón, Luis F. Ospina, Actividad antinflamatoria de extractos y fracciones obtenidas de cálices de Physalis peruviana L. , Biomédica: Vol. 27 Núm. 1 (2007)
- Ana María Vásquez, Alberto Tobón, Mecanismos de patogenia en la malaria por Plasmodium falciparum , Biomédica: Vol. 32 (2012): Suplemento 1, Malaria
- Jorge Andrés Cuellar, Alejandro Hernández, Enrique Villegas, Jorge Enrique Gómez, Eficiencia de cultivo in vitro de Toxoplasma gondii en las líneas celulares THP1 y Vero , Biomédica: Vol. 32 Núm. 3 (2012)
- Juan Carlos Villa-Camacho, Juan Camilo Vargas-Zambrano, John Mario González, Modelo de detección de anticuerpos neutralizantes contra IFN-β mediante citometría de flujo , Biomédica: Vol. 32 Núm. 4 (2012)
- Jose Mateus, Paola Lasso, John Mario González, Concepción Judith Puerta, Adriana Cuéllar, Diseño de un panel multicolor para evaluar moléculas intracelulares y de superficie mediante citometría de flujo , Biomédica: Vol. 33 Núm. 4 (2013)
- Sandra Milena Quijano, María Mercedes Torres, Liliana Edith Vásquez, Gina Elizabeth Cuellar, Martha Liliana Romero, Edna Liliana Martín, Adriana Linares, Silverio Castaño, Isabel Cristina Sarmiento, Edgar Cabrera, Gloria Inés Uribe, Rafael Enrique Andrade, Carlos Eugenio Saavedra, Correlación de la t(9;22), t(12;21) e hiperdiploidía de ADN con el inmunofenotipo y la tasa de proliferación de células B neoplásicas en niños con leucemia linfoblástica aguda de precursores B , Biomédica: Vol. 33 Núm. 3 (2013)
- Luis Ángel Villar, Rosa Margarita Gélvez, Jairo Antonio Rodríguez, Doris Salgado, Beatriz Parra, Lyda Osorio, Irene Bosch, Biomarcadores pronósticos de gravedad del dengue , Biomédica: Vol. 33 (2013): Suplemento 1, Fiebres hemorrágicas
- Viviana Marcela Rodríguez, Adriana Cuéllar, Lyda Marcela Cuspoca, Carmen Lucía Contreras, Marcela Mercado, Alberto Gómez, Determinación fenotípica de subpoblaciones de células madre derivadas de sangre de cordón umbilical. , Biomédica: Vol. 26 Núm. 1 (2006)
- Fabián Jaimes, Gisela de la Rosa, Anticoagulación y sepsis, la oportunidad para un nuevo uso de la heparina? , Biomédica: Vol. 26 Núm. 1 (2006)
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























