Detección de Treponema pallidum subespecie pallidum para el diagnóstico de sífilis congénita mediante reacción en cadena de la polimerasa anidada
Resumen
Introducción. La sífilis es una enfermedad producida por Treponema pallidum subespecie pallidum cuya incidencia mundial es de 12 millones de casos por año, aproximadamente; de estos, más de dos millones se presentan en mujeres gestantes, siendo la sífilis congénita la complicación más grave de esta infección en el embarazo.
Objetivo. Detectar la presencia de T. pallidum subespecie pallidum en muestras clínicas para el diagnóstico de sífilis congénita mediante reacción en cadena de la polimerasa (PCR) anidada y determinar su concordancia con las pruebas serológicas.
Materiales y métodos. Mediante PCR convencional y anidada, se amplificaron tres genes diana (polA, 16S ADNr y TpN47) y se confirmaron los productos de amplificación de los genes TpN47 y polA por secuenciación. Las pruebas serológicas empleadas fueron la VDRL (Venereal Disease Research Laboratory), la de reagina plasmática rápida (Rapid Plasma Reagin, RPR) y la de aglutinación de partículas para Treponema pallidum (Treponema pallidum Particle Agglutination Assay, TPPA).
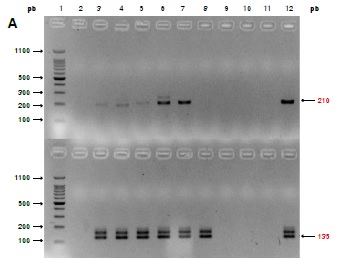
Resultados. La sensibilidad para la PCR convencional fue de 52 pg y, para la PCR anidada, de 0,52 pg. La especificidad con los iniciadores TpN47 y polA fue de 100 %; los resultados de la secuenciación mostraron una identidad de 97 % con T. pallidum. En 70 % de las muestras, los resultados de las pruebas serológicas y la PCR anidada concordaron.
Conclusión. El gen TpN47 resultó ser el mejor blanco molecular para la identificación de T. pallidum. La PCR anidada se presenta como una alternativa de diagnóstico molecular promisoria para el diagnóstico de sífilis congénita.
Descargas
Referencias bibliográficas
Grange P, Gressier L, Dion P, Farhi D, Benhaddou N, Gerhardt P, et al. Evaluation of a PCR test for detection of Treponema pallidum in swabs and blood. J Clin Microbiol. 2012;50:546-52. https://doi.org/10.1128/JCM.00702-11
Casal D, Silva O, Costa I, Araújo C, Corvelo C. Molecular detection of Treponema pallidum sp. pallidum in blood samples of VDRL-seroreactive women with lethal pregnancy outcomes: A retrospective observational study in northern Brazil. Rev Soc Bras Med Trop. 2011;44:451-6. https://doi.org/10.1590/S0037-86822011005000047
Buffet M, Grange P, Gerhardt P, Carlotti A, Calvez V, Bianchi A, et al. Diagnosing Treponema pallidum in secondary syphilis by PCR and immunohistochemistry. J Invest Dermatol. 2007;127:2345-50. https://doi.org/10.1038/sj.jid.5700888
De la Hoz F, Martínez M, Pacheco O, Quijada H, Beltrán M, Ramírez C. Protocolo de vigilancia en salud pública. Sífilis gestacional y sífilis congénita. Bogotá: Instituto Nacional de Salud; 2015. p. 2-3.
Valderrama J, Zacarías F, Mazin R. Sífilis materna y sífilis congénita en América Latina: un problema grave de solución sencilla. Rev Panam Salud Pública. 2004;16:211-7. https://doi.org/10.1590/S1020-49892004000900012
Casas-P RL, Rodríguez M, Rivas J. Sífilis y embarazo: ¿cómo diagnosticar y tratar oportunamente? Rev Colomb Obstet Ginecol. 2009;60:49-56.
Organización Panamericana de la Salud. Guía clínica para la eliminación de la transmisión materno-infantil del VIH y de la sífilis congénita en América Latina y el Caribe. Washington, D.C.: OPS; 2009.
Díaz LA. Sífilis gestacional: un problema de salud pública. Rev Fac Med. 2011;59:163-5.
Cruz AR. Situación de la sífilis gestacional y congénita en Colombia, un desafío al Sistema General de Seguridad Social en Salud. Rev Colomb Obstet Ginecol. 2012;63:308-11.
Cifuentes M, Ojeda C. Sífilis congénita en el Instituto Materno Infantil-Hospital La Victoria, Bogotá. Rev Salud Pública. 2013;15:434-45.
Herring A, Ballard R, Mabey D, Peeling R. Evaluation of rapid diagnostic tests: Syphilis. Nat Rev Microbiol. 2006;4 (Suppl.):S33-40. https://doi.org/10.1038/nrmicro1563
Luu M, Ham C, Kamb M, Caffe S, Hoover K, Pérez F. Syphilis testing in antenatal care: Policies and practices among laboratories in the Americas. Int J Gynecol Obstet. 2015;130(Suppl.1):S37-42. https://doi.org/10.1016/j.ijgo.2015.04.011
Martin I, Weiming G, Tsang R. Macrolide resistance and molecular types of Treponema pallidum causing primary syphilis in Shanghai, China. Clin Infect Dis. 2009;49:515-21. https://doi.org/10.1086/600878
Ham D, Lin C, Newman L, Wijesooriya N, Kamb M. Improving global estimates of syphilis in pregnancy by diagnostic test type: A systematic review and meta-analysis. Int J Gynecol Obstet. 2015;130(Suppl.1):S10-4. https://doi.org/10.1016/j.ijgo.2015.04.012
Singh A, Levett P, Fonseca K, Jayaraman G, Lee B. Canadian Public Health Laboratory Network laboratory guidelines for congenital syphilis and syphilis screening in pregnant women in Canada. Canad J Infect Dis Med Microbiol. 2015;26(Suppl.A):23A-8. https://doi.org/10.1155/2015/589085
Martin I, Tsang R, Sutherland K, Tilley P, Read R, Anderson B, et al. Molecular characterization of syphilis in patients in Canada: Azithromycin resistance and detection of Treponema pallidum DNA in whole-blood samples versus ulcerative swabs. J Clin Microbiol. 2009;47:1668-73. https://doi.org/10.1128/JCM.02392-08
Heymans R, Helm J, Vries C, Fennema A, Coutinho A, Bruisten M. Clinical value of Treponema pallidum real-time PCR for diagnosis of syphilis. J Clin Microbiol. 2010;48:497-502. https://doi.org/10.1128/JCM.00720-09
Sampedro A, Martínez LA, Teatino PM, Rodríguez-Granger J. Diagnosis of congenital infection. Enferm Infecc Microbiol Clin. 2011;29:15-20. https://doi.org/10.1016/S0213-005X(11)70039-8
Cejková D, Zobaníková M, Chen L, Pospíšilová P, Strouhal M, Qin X, et al. Whole genome sequences of three Treponema pallidum ssp. pertenue strains: Yaws and syphilis treponemes differ in less than 0.2% of the genome sequence. PLoS Negl Trop Dis. 2012;6:e1471. https://doi.org/10.1371/journal.pntd.0001471
Promega. Technical Manual, Wizard Genomic DNA Purification Kit®. Fecha de consulta: 5 de septiembre de 2016. Disponible en: https://www.promega.com/~/media/files/resources/protocols/technical%20manuals/0/wizard%20genomic%20dna%20purification%20kit%20protocol.pdf
Pinilla G, Chavarro B, Moreno N, Navarrete J, Muñoz L. Determinación de los genes, 16S ADNr, polA y TpN47, en la detección de Treponema pallidum subsp. pallidum para el diagnóstico de sífilis congénita. NOVA. 2015;13:17-25.
QIAGEN. QIAamp DNA Mini Kit® and QIAamp DNA Blood Mini Kit® Handbook 2013. Fecha de consulta: 15 de marzo de 2015. Disponible en: http://emerald.tufts.edu/~mcourt01/Documents/QIAGEN_protocol.pdf
Macrogen. Normal Automatic Sequencing. Fecha de consulta: 10 de octubre de 2015. Disponible en: http://www.macrogen.com/download/Standard_Seq_Brochure.pdf
Thermo Fisher. VDRL Test Kit®. Fecha de consulta: 2 de febrero de 2015. Disponible en: http://tools.thermofisher.com/content/sfs/manuals/X4988B-ES.pdf
BioKit. Rapid test for the qualitative and quantitative detection of syphilis in serum or plasma. Fecha de consulta: 2 de febrero de 2015. Disponible en: http://docplayer.es/35836985-Rpr-reditest-rapid-test-for-the-qualitative-andquantitative-detection-of-syphilis-in-serum-or-plasma.html
Fujirebio T. Serodia-TPPA. Fecha de consulta: 22 de marzo de 2015. Disponible en: http://www.fdi.com/documents/products/inserts/PROOF%20POLLOCK%20Serodia_TP_PA_Sheet%20020912.pdf
Chowdhary N, Rani K, Mukunda K, Kiran K. Early detection of congenital syphilis. J Indian Soc Pedod Prev Dent. 2014;32:333-7. https://doi.org/10.4103/0970-4388.140969
Ramos JM, León R, Andreu M, de las Parras ER, Rodríguez-Díaz JC, Esteban Á, et al. Serological study of Trypanosoma cruzi, Strongyloides stercoralis, HIV, human T cell lymphotropic virus (HTLV) and syphilis infections in asymptomatic Latin American immigrants in Spain. Trans R Soc Trop Med Hyg. 2015;109:447-53. https://doi.org/10.1093/trstmh/trv043
Gayet-Ageron A, Combescure C, Lautenschlager S, Ninet B, Perneger TV. Comparison of diagnostic accuracy of PCR targeting the 47-kilodalton protein membrane gene of Treponema pallidum and PCR targeting the DNA polymerase I gene: Systematic review and meta-analysis. J Clin Microbiol. 2015;53:3522-9. https://doi.org/10.1128/JCM.01619-15
Noda A, Blanco O, Correa C, Pérez L, Kourí V, Rodríguez I. Etiology of genital ulcer disease in male patients attending a sexually transmitted diseases clinic: First assessment in Cuba. Sex Transm Dis. 2016;43:494-7. https://doi.org/10.1097/OLQ.0000000000000470
Castro R, Águas MJ, Batista T, Araújo C, Mansinho K, Pereira F da L. Detection of Treponema pallidum sp. pallidum DNA in cerebrospinal fluid (CSF) by two PCR techniques. J Clin Lab Anal. 2016;30:628-32. https://doi.org/10.1002/jcla.21913
Liu H, Rodes B, Chen C-Y, Steiner B. New tests for syphilis: Rational design of a PCR method for detection of Treponema pallidum in clinical specimens using unique regions of the DNA polymerase I gene. J Clin Microbiol. 2001;39:1941-6. https://doi.org/10.1128/JCM.39.5.1941-1946.2001
Pope V, Fox K, Liu H, Marfin A, Leone P, Seña C, et al. Molecular subtyping of Treponema pallidum from North and South Carolina. J Clin Microbiol. 2005;43:3743-6. https://doi.org/10.1128/JCM.43.8.3743-3746.2005
Castro R, Prieto E, Aguas M, Manata M, Botas J, Martins P. Molecular subtyping of Treponema pallidum subsp. pallidum in Lisbon, Portugal. J Clin Microbiol. 2009;47:2510-2. https://doi.org/10.1128/JCM.00287-08
Větrovský T, Baldrian P. The variability of the 16S rRNA gene in bacterial genomes and its consequences for bacterial community analyses. PLoS One. 2013;8:e57923.
Grillová L, Pĕtrošová H, Mikalová L, Strnadel R, Dastychová E, Kuklová I, et al. Molecular typing of Treponema pallidum in the Czech Republic during 2011 to 2013: Increased prevalence of identified genotypes and of isolates with macrolide resistance. J Clin Microbiol. 2014;52:3693-700. https://doi.org/10.1128/JCM.01292-14
Leslie E, Azzato F, Karapanagiotidis T, Leydon J, Fyfe J. Development of a real-time PCR assay to detect Treponema pallidum in clinical specimens and assessment of the assay’s performance by comparison with serological testing. J Clin Microbiol. 2007;45:93-6. https://doi.org/10.1128/JCM.01578-06
Bruisten M, Cairo I, Fennema H, Pijl A, Buimer M, Peerbooms G, et al. Diagnosing genital ulcer disease in a clinic for sexually transmitted diseases in Amsterdam, The Netherlands. J Clin Microbiol. 2001;39:601-5. https://doi.org/10.1128/JCM.39.2.601-605.2001
Mendoza N, Jaramillo C, Guhl F, Padilla J, Rentería M. Diagnóstico de malaria por el método de la PCR anidada. Biomédica. 2001;21:320-7. https://doi.org/10.7705/biomedica.v21i4.1124
Algunos artículos similares:
- Liliana Torcoroma García, Jhancy Rocío Aguilar, Marly Yojhana Bueno , Erika Marcela Moreno, Herminia Ramírez , Nelson Daza , Desacuerdo entre la PCR y la serología en el diagnóstico de la infección por Trypanosoma cruzi en donantes de una región endémica de Colombia , Biomédica: Vol. 41 Núm. Supl. 1 (2021): Mayo, Parasitología médica
- Yolanda Cifuentes, Martha Isabel Murcia, Jorge Piar, Patricia Pardo, Microcalcificaciones cerebrales en un recién nacido con tuberculosis congénita , Biomédica: Vol. 36 Núm. 1 (2016)
- Rubén Santiago Nicholls, Zulma Milena Cucunubá, Angélica Knudson, Astrid Carolina Flórez, Marleny Montilla, Concepción Judith Puerta, Paula Ximena Pavía, Enfermedad de Chagas aguda en Colombia, una entidad poco sospechada. Informe de 10 casos presentados en el periodo 2002 a 2005 , Biomédica: Vol. 27 Núm. 1esp (2007): Enfermedad de Chagas
- Beatriz E. Orozco-Sebá, Diego Viasus , Esperanza Meléndez , Jairo Fuentes , José Tovar , Elkin A. Amado , Daniela Loaiza , Colestasis intrahepática por Treponema pallidum en paciente inmunocompetente , Biomédica: Vol. 43 Núm. 2 (2023)
- Martine Bonnaure-Mallet, Paula Juliana Pérez-Chaparro, Patrice Gracieux, Vincent Meuric, Zohreh Tamanai-Shacoori, Jaime Eduardo Castellanos, Distribución de los genotipos de fimA en cepas de Porphyromonas gingivalis aisladas de placas subgingivales y de sangre durante bacteriemias , Biomédica: Vol. 29 Núm. 2 (2009)
- Diego Fernando Zea, Martín Prager, Roger Adrian Figueroa, María Consuelo Miranda, Complicación mucosa de la leishmaniasis cutánea , Biomédica: Vol. 29 Núm. 1 (2009)
- Ana Margarita Montalvo, Lianet Monzote, Jorge Fraga, Ivón Montano, Carlos Muskus, Marcel Marín, Simonne De Donck, Iván Darío Vélez, Jean Claude Dujardin, PCR-RFLP y RAPD para la tipificación de Leishmania neotropical , Biomédica: Vol. 28 Núm. 4 (2008)
- Concepción Judith Puerta, Johana María Guevara, Paula Ximena Pavía, Marleny Montilla, Rubén Santiago Nicholls, Edgar Parra, Yuli Katherine Barrera, Evaluación de las pruebas de PCR TcH2AF-R y S35-S36 para la detección de Trypanosoma cruzi en tejido cardiaco de ratón , Biomédica: Vol. 28 Núm. 4 (2008)
- Marcel Marín, Yudy Alexandra Aguilar, José Robinson Ramírez, Omar Triana, Carlos Enrique Muskus, El análisis molecular y el inmunogénico sugieren la ausencia de las proteínas hidrofílicas de superficie en Leishmania (Viannia) panamensis , Biomédica: Vol. 28 Núm. 3 (2008)
- Concepción Judith Puerta, Paula Ximena Pavia, Marleny Montilla, Carolina Flórez, Giomar Herrera, Juan Manuel Ospina, Fred Manrique, Rubén Santiago Nicholls, Reporte del primer caso de enfermedad de Chagas transplacentaria analizado por AP-PCR en Moniquirá, Boyacá , Biomédica: Vol. 29 Núm. 4 (2009)
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























