Detección de Toxoplasma gondii en agua para el consumo humano proveniente de jagüeyes del área rural del municipio de Sincelejo
Resumen
Introducción. La toxoplasmosis es una zoonosis que se transmite por vía oral al consumir alimentos contaminados con cualquier forma infectiva de Toxoplasma gondii. Su transmisión por agua ha sido documentada en varios países, incluido Colombia. Al no disponer de agua potable, la población rural de Sincelejo podría estar en riesgo de contraer toxoplasmosis por esta vía.
Objetivo. Evaluar la contaminación por T. gondii del agua para consumo humano proveniente de jagüeyes de la zona rural de Sincelejo y establecer su relación con diferentes determinantes sociales de la salud en el área de estudio.
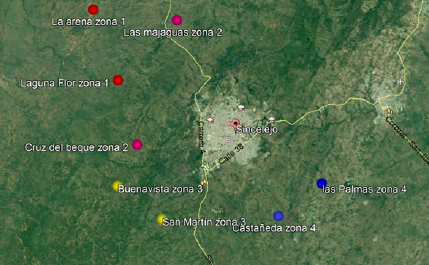
Materiales y métodos. Mediante PCR anidada, se evaluaron 96 muestras de agua obtenidas en 48 fincas ubicadas en ocho corregimientos rurales de Sincelejo. En cada finca se obtuvieron dos muestras: una de agua cruda de jagüey y otra destinada al consumo directo. En cada finca se hizo una encuesta para recolectar información sobre características físicas de la vivienda, presencia de gatos, y disponibilidad de agua y sus usos. Las relaciones estadísticas se evaluaron con el test de Fisher.
Resultados. De las 96 muestras analizadas, 13 resultaron contaminadas con T. gondii (13,5 %): nueve de agua cruda y cuatro de agua para el consumo directo. No se encontró asociación estadística entre las muestras positivas y los determinantes sociales de la salud evaluados (p>0,05).
Conclusión. La población rural de Sincelejo podría estar en riesgo de contraer toxoplasmosis por el uso y consumo del agua proveniente de sus jagüeyes. La contaminación de estos cuerpos de agua por T. gondii puede estar influenciada por otros determinantes sociales de la salud no contemplados aquí.
Descargas
Referencias bibliográficas
Abu-Madi MA, Al-Molawi N, Behnke JM. Seroprevalence and epidemiological correlates of Toxoplasma gondii infections among patients referred for hospital-based serological testing in Doha, Qatar. Parasit Vectors. 2008;1:1-9. https://doi.org/10.1186/1756-3305-1-39
Carrada TB. Toxoplasmosis: parasitosis reemergente del nuevo milenio. Rev Mex Patol Clin. 2005;52:151-62.
Sánchez R, Cobos D, Miranda A, Goya Y, Miranda A. Aspectos básicos sobre la patogenia, respuesta inmune y bioseguridad en el trabajo con el Toxoplasma gondii. Correo Científico Médico. 2012;16:1-16.
Simon A, Bigras M, Rousseau AN, Dubey JP, Ogden NH. Spatiotemporal dynamics of Toxoplasma gondii infection in Canadian lynx (Lynx canadensis) in western Québec,
Canada. J Wildl Dis. 2013;49:39-48. https://doi.org/10.7589/2012-02-048
Gómez F. Estudio sobre la toxoplasmosis en Andorra y el Alt Urgell (tesis). Barcelona: Universidad de Barcelona; 2004.
Alvarado F. Toxoplasmosis en el Inmunosuprimido. Rev Salud Pública. 2002;4:31-4.
Lizarazo J, Castro F, De Arco M, Chaves C, Peña Y. Infecciones oportunistas del sistema nervioso central en pacientes con VIH atendidos en el Hospital Universitario Erasmo Meoz, Cúcuta, 1995-2005. Infectio. 2006;10:226-31.
Ávila G, González G. Algunas manifestaciones neurológicas del síndrome de inmunodeficiencia adquirida (sida) en pacientes del hospital universitario Hernando Moncaleano Perdomo de Neiva, 2001 -2004. Acta Biológica Colombiana. 2007;23:90-4.
Campo DM, Discuviche MA, Blanco PJ, Montero YM, Orozco KE, Assia YM. Detección de Toxoplasma gondii por amplificación del gen B1 en carnes de consumo humano. Infectio. 2014;18:93-9. https://doi.org/10.1016/j.infect.2014.05.001
Giraldo M. Toxoplasmosis. Medicina & Laboratorio. 2008;14:359-75.
Cortés J, Gómez J, Silva P, Arévalo L, Arévalo I, Álvarez M, et al. Guía de atención integral para la prevención, detección temprana y tratamiento de las complicaciones del embarazo, parto y puerperio: sección toxoplasmosis en el embarazo. Infectio. 2012;16:230-46. https://doi.org/10.1016/S0123-9392(12)70018-8
Pino LE, Salinas JE. Descripción de un brote epidémico de toxoplasmosis aguda en pacientes inmunocompetentes miembros de las fuerzas militares de Colombia durante
operaciones de selva. Infectio. 2009;13:83-91. https://doi.org/10.1016/S0123-9392(09)70729-5
Arcia C. Detección molecular de comunidades microbianas en agua para el consumo humano en el municipio de sincelejo, Sucre- Colombia (tesis). Sincelejo: Universidad de Córdoba; 2016.
Sánchez C. Detección y caracterización molecular de los parásitos de interés en salud pública: Giardia duodenalis, Cryptosporidium spp., Cyclospora cayetanensis, Toxoplasma gondii y Entamoeba histolytica, en agua cruda y tratada de cuatro plantas potabilizadoras del departamento de Nariño (Colombia) (tesis). Bogotá: Universidad Nacional de Colombia; 2017.
Triviño J, Lora F, Zuluaga J, Gómez, J. Detection by PCR of pathogenic protozoa in raw and drinkable water samples in Colombia. Parasitol Res. 2016;115:1789-97. https://doi.org/10.1007/s00436-016-4917-5
Luna JC, Zamora A, Hernández-Arango N, Muñoz-Sánchez D, Pinzón MI, Cortés-Vecino JA, et al. Food safety assessment and risk for toxoplasmosis in school restaurants in Armenia, Colombia. Parasitol Res. 2019;118:3449-57. https://doi.org/10.1007/s00436-019-06473-w
Ballut-Dajud G, Monroy-Pineda MC. Los jagüeyes del municipio de Sincelejo, Sucre, Colombia. Rev Colomb Cienc Anim. 2015;7:80-3. https://doi.org/10.24188/recia.v7.n1.2015.426
Sroka J, Wójcik-Fatla A, Dutkiewicz J. Occurrence of Toxoplasma gondii in water from wells located on farms. Ann Agric Environ Med. 2006;13:169-75.
Isaac-Renton J, Bowie WR, King A, Irwin GS, Ong CS, Fung CP, et al. Detection of Toxoplasma gondii oocysts in drinking water. Appl Environ Microbiol. 1998;64:2278-80. https://doi.org/10.1128/AEM.64.6.2278-2280.1998
Blanco PJ, Assia YM, Montero YM, Orozco KE. ELFA IgG anti-Toxoplasma y PCR anidada para el diagnóstico de toxoplasmosis en mujeres gestantes de Sincelejo, Colombia. Infectio. 2011;15:253-8. https://doi.org/10.1016/S0123-9392(11)70739-1
Benenson MW, Takafuji ET, Lemon SM, Greenup RL, Sulzer AJ. Oocyst-transmitted toxoplasmosis associated with ingestion of contaminated water. N Engl J Med. 1982;307:666-9. https://doi.org/10.1056/NEJM198209093071107
Bowie WR, King AS, Werker DH, Isaac-Renton JL, Bell A, Eng SB, et al. Outbreak of toxoplasmosis associated with municipal drinking water. Lancet. 1997;350:173-7. https://doi.org/10.1016/s0140-6736(96)11105-3
Aramini JJ, Stephen C, Dubey JP, Engelstoft C, Schwantje H, Ribble CS. Potential contamination of drinking water with Toxoplasma gondii oocysts. Epidemiol Infect. 1999;122:305-15. https://doi.org/10.1017/s0950268899002113
De Moura L, García LM, Wada MY, Jones JL, Tuboi SH, Carmo EH, et al. Waterborne, toxoplasmosis, Brazil, from field to gene. Emerg Infect Dis. 2006;12:326-9. https://doi.org/10.3201/eid1202.041115
Balasundaram MB, Andavar R, Palaniswamy M, Venkatapathy N. Outbreak of acquired ocular toxoplasmosis involving 248 patients. Arch. Ophthalmol. 2010;128:28-32. https://doi.org/10.1001/archophthalmol.2009.354
Adamska M. Molecular detection of Toxoplasma gondii in natural surface water bodies in Poland. J Water Health. 2018;16:657-60. https://doi.org/.10.2166/wh.2018.236
Ćirković V, Uzelac A, Miličić D, Klun I, Djurković-Djaković O. First detection of Toxoplasma gondii (Nicolle & Manceaux, 1908) (Eucoccidiorida: Sarcocystidae) in river waters in Serbia. Acta Zool Bulg. 2020;7:79-83. http://www.acta-zoologica-bulgarica.eu/Suppl_15_15
Galvani AT, Guarnieri AP, Padula JA, Funada MR, Silva R, Zanoli MI, et al. Real-time PCR detection of Toxoplasma gondii in surface water samples in São Paulo, Brazil. Parasitol Res. 2019;118:631-40. https://doi.org/10.1007/s00436-018-6185-z
Ministerio del Interior de Colombia. Convenio Interadministrativo N° M-923 de 2013 celebrado entre la nación, ministerio del interior y el Cabildo Mayor Regional del Pueblo Zinú: diagnóstico comunitario y líneas de acción para el plan de salvaguarda étnica del pueblo Zinú, capítulo Córdoba-Sucre y dispersos. Fecha de consulta: 25 de marzo de 2020. Disponible en: https://siic.mininterior.gov.co/sites/default/files/pueblo_zenu_-_diagnostico_comunitario_tomo_1.pdf
Castaño C, González J, Ange C, Zárrate D, Vela M. Ecología y conservación de felinos y presas en el Caribe Colombiano. En: Castaño C, González J, Zárrate D, Ange C, Vela I, editores. Plan de Conservación de Felinos del Caribe colombiano: Los felinos y su papel en la planificación regional integral basada en especies clave. Santa Marta: Fundación Herencia ambiental Caribe, ProCAT Colombia, The Sierra to Sea Institute.; 2013. p. 1-233.
Algunos artículos similares:
- Liliana Jazmín Cortés, Sofía Duque, Myriam Consuelo López, Diego Moncada, Diego Molina, Jorge Enrique Gómez-Marín, María Luz Gunturiz, Polimorfismos en los genes de dihidrofolato-reductasa (dhfr) y dihidropteroato-sintasa (dhps) y modelado estructural del gen dhps en aislamientos colombianos de Toxoplasma gondii , Biomédica: Vol. 34 Núm. 4 (2014)
- Mercedes Salcedo-Cifuentes, Jesús Cabrera, Yesid Cuesta-Astroz, Edwin Carrascal, Yoshito Eizuru, Martha C. Domínguez, Adalberto Sánchez, Felipe García-Vallejo, Expansión clónica y caracterización genómica del proceso de integración del virus linfotrópico humano tipo I en la leucemia/linfoma de células T en adultos , Biomédica: Vol. 29 Núm. 2 (2009)
- Martine Bonnaure-Mallet, Paula Juliana Pérez-Chaparro, Patrice Gracieux, Vincent Meuric, Zohreh Tamanai-Shacoori, Jaime Eduardo Castellanos, Distribución de los genotipos de fimA en cepas de Porphyromonas gingivalis aisladas de placas subgingivales y de sangre durante bacteriemias , Biomédica: Vol. 29 Núm. 2 (2009)
- Diego Fernando Zea, Martín Prager, Roger Adrian Figueroa, María Consuelo Miranda, Complicación mucosa de la leishmaniasis cutánea , Biomédica: Vol. 29 Núm. 1 (2009)
- Ana Margarita Montalvo, Lianet Monzote, Jorge Fraga, Ivón Montano, Carlos Muskus, Marcel Marín, Simonne De Donck, Iván Darío Vélez, Jean Claude Dujardin, PCR-RFLP y RAPD para la tipificación de Leishmania neotropical , Biomédica: Vol. 28 Núm. 4 (2008)
- Concepción Judith Puerta, Johana María Guevara, Paula Ximena Pavía, Marleny Montilla, Rubén Santiago Nicholls, Edgar Parra, Yuli Katherine Barrera, Evaluación de las pruebas de PCR TcH2AF-R y S35-S36 para la detección de Trypanosoma cruzi en tejido cardiaco de ratón , Biomédica: Vol. 28 Núm. 4 (2008)
- Marcel Marín, Yudy Alexandra Aguilar, José Robinson Ramírez, Omar Triana, Carlos Enrique Muskus, El análisis molecular y el inmunogénico sugieren la ausencia de las proteínas hidrofílicas de superficie en Leishmania (Viannia) panamensis , Biomédica: Vol. 28 Núm. 3 (2008)
- Astrid Elena Montoya, José Menco, Natalia Osorio, Maria Alejandra Zuluaga, Juliana Duque, Giovanny Torres, Marcos Restrepo, Concordancia entre gota gruesa, inmunocromatografía y reacción en cadena de la polimerasa para el diagnóstico de malaria , Biomédica: Vol. 28 Núm. 2 (2008)
- Concepción Judith Puerta, Paula Ximena Pavia, Marleny Montilla, Carolina Flórez, Giomar Herrera, Juan Manuel Ospina, Fred Manrique, Rubén Santiago Nicholls, Reporte del primer caso de enfermedad de Chagas transplacentaria analizado por AP-PCR en Moniquirá, Boyacá , Biomédica: Vol. 29 Núm. 4 (2009)
- María Teresa Arango, Carlos Jaramillo, María Camila Montealegre, Mabel Helena Bohórquez, María del Pilar Delgado, Genotipificación de los polimorfismos -511, -31 y +3954 del gen de la interleucina-1β humana en una población colombiana con cuadro de dispepsia , Biomédica: Vol. 30 Núm. 2 (2010)
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























